Értékelések
Nincs még értékelés. Legyél Te az első!
Legnépszerűbb doksik ebben a kategóriában
Tartalmi kivonat
SZOMATOSZENZOROS MŰKÖDÉS AGYI ELEKTROMOS TEVÉKENYSÉG ÉBRESZTÉS ÉBRENLÉT – ALVÁS Dr. Eke András egyetemi docens Egyetemi jegyzet (2. elektronikus kiadása) Semmelweis Egyetem Klinikai Kísérleti Kutató- és Humán Élettani Intézet 2001. RECEPTORFIZIOLÓGIA Általános bevezetés A receptorok működésének lényege az, hogy átalakítják a külső és a belső környezetből szervezetünket érő energiabehatásokat (ingereket), és így lehetővé teszik, hogy azok a perifériás és központi idegrendszerbe jussanak, ott feldolgozást nyerjenek, és így kialakulhasson a szervezetünket ért ingerbehatásra a biológiailag célszerű válasz. Alapfogalmak: • • • • • • inger – ingerület – érzet modalitás ingerintenzitás (erősség) időtartam gyakoriság, frekvencia lokalizáció A szervezetet, illetve annak részeit egyidejűleg különféle energia-behatások együttese éri. Ebből az ingertömegből egy-egy adott energiafajta
felvételére azért van mód, mert az egyes receptorféleségek felépítésük és működésük alapján specializálódtak az adott energiaforma (mechanikai, kémiai, hő stb.) felvételére A receptorok egy része érzékszerveket képez (szem, fül), és speciális ingermodalitás felvételével komplex érzékelési funkciók megvalósításában vesz részt (fény–látás, hang–hallás). Ezeknek a receptoroknak a működését az élettan megfelelő fejezetei tárgyalják. A receptorok osztályozása A receptorok osztályozása különféle szempontok szerint történhet: • • • • • • inger forrása: exteroceptorok (bőr, szem, fül stb.), interoceptorok (kemo-, baro-, proprioceptorok) ingerlő energia fajtája (mechano-, thermo-, noci-, foto-, kemoreceptorok) kialakuló érzetféleség (tapintás, hideg–meleg, fájdalom, foto, halló, ízlelő, szagló) adaptáció (gyors és lassú) lokalizáció (felületi, mély, viszcerális, speciális) egyéb (tele-
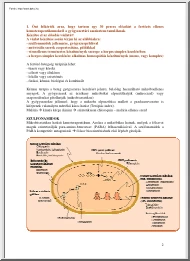
vs. kontakt receptorok) 2 MECHANORECEPTOR KEMORECEPTOR FOTORECEPTOR 1. ábra A receptormembrán tulajdonságának megváltozása inger behatására különféle receptorok esetében. A közös elem, mely a receptorban elindítja az ingerületi folyamatot, a membrán ionpermeabilitásának növekedése, vagy csökkenése. (Berne and Levy, Physiology, Fourth Edition, Fig. 7-2 alapján) 3 A receptorokban az inger behatása jelet hoz létre Az érzékelés lényegi mozzanata az energiaátvitel (transzdukció), melynek során az inger behatására a receptorsejt mebrántulajdonsága megváltozik. A transzdukció eltérő modalitások esetében is az érzékelési folyamatban a közös, indító elem (1. ábra). Alapfogalmak: • • • • adekvát inger az ingerlő energiaátvitel (transzdukció) adaptáció kódolás A receptor számára adekvát inger az energiának az a fajtája, melyből már egy minimálisan elégséges mennyiség is kiváltja a receptorra jellemző
ingerület-leadást, és előidézi a receptor által kódolt modalitására jellemző érzetet. Egy receptor specificitása egyrészt a receptor sajátos szerkezetéből, másrészt pedig sajátos működéséből adódik. Ezek együttesen határozzák meg, hogy egy adott receptor számára mi az adekvát inger, tehát mi is az, amit a receptor érzékel. Az energia-transzdukció két lépésben történik. Első lépésben az ingerlő energia kapcsolatba lép a receptorsejt membránjával, és annak ionpermeabilitását megváltoztatja (1 és 2. ábra) Ennek következtében a receptor ún transducer régióján egy elsődleges helyi válasz, a receptorpotenciál (RP) alakul ki (3. ábra) Ha a receptorpotenciál meghaladja a receptor membránjára jellemző küszöbpotenciál értékét, akkor a receptor sejtmembránjának egy proximálisabb részén (generátor régió) kialakul az akciós potenciál (AP) (3. ábra) Minél nagyobb az ingerintenzitás (I), annál nagyobb a RP
amplitúdója és így az APsorozat frekvenciája is (4. ábra) I és RP közötti összefüggést a Steven-féle hatványtörvény írja le: 4 2. ábra Egy mechanoreceptor ingerlése a receptor centrumában található idegvégződés membránját deformálja, ami a membránpermeabilitást megnövelve a legközelebbi Ranvierféle befűződés irányában lokális ionáramot generál. Tovaterjedő akciós potenciál (AP) 3. ábra A receptorpotenciál az inger hatására + + + + + + + + + + + + + + + + a receptor + + + transzducer + + régióján jelenik + + + + + + + + + + + + + + meg és terjed át a proximálisan Transzducer régió AP-generáló régió elhelyezkedő akciós potenciál generáló régióra. E két régió egymáshoz való kapcsolódásának jellege adja részbeni magyarázatát az adott receptorra jellemző adaptációnak. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-3 alapján) Akciós potenciálok mV Receptorpotenciál -60
-90 Nyugalmi membránpotenciál Küszöbpotenciál 0 100 IDŐ (msec) 4. ábra Ingerlés hatására az idegvégződés membránja depolarizálódik. A depolarizáció – a receptorpotenciál – mértéke arányos az inger intenzitásával. Ha a receptorpotenciál meghaladja az adott receptorra jellemző küszöbértéket, akkor akciós potenciál keletkezik, melynek frekvenciája arányos a receptorpotenciállal, és így az ingerintenzitással. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-2 alapján) 5 VRP = k ( I − I 0 ) n ahol VRP = a receptorpotenciál nagysága k = konstans I = ingerintenzitás Io = küszöbintenzitás n = hatványkitevő, egy adott modalitásra jellemző konstans Ez az összefüggés még ismeretes egy kevésbé pontos, jóval korábban leírt alakban is (Fechner-törvény). VRP = k log I Io A hatványkitevő, n, értéke egy-egy modalitásra és receptorféleségre jellemző állandó, mely lehet n<1, n~1
vagy n>1, és ami meghatározza, hogy az adott receptor mely intenzitástartományban mutat kis – illetve melyben nagy érzékenységet (5. ábra) Látható, hogy egy bőr mechanoreceptor (n<1) igen érzékeny a kis energiatartományokban, és így igen alkalmas finom mechanikai ingerek detektálására (pl. bőr simítása) A hideg receptorok (n~1) válaszában megmutatkozó érzékenység nem függ az ingerintezitástól, míg a nociceptorok (n>1) a károsító behatás intenzitásának fokozódásával növekszik, mely egyezik azon tapasztalatunkkal, hogy ilyenkor a fájdalom jelentősen fokozódik. A receptorok egyrészt anatómiai felépítésük, másrészt a receptorfolyamatok eltérő természete miatt különböző mértékű adaptációt mutatnak. Ha folyamatos ingerbehatás mellett az AP-frekvencia az időben gyorsan csökken, a receptor gyors adaptációt mutat (fázisos vagy dinamikus receptor), ha az AP-frekvencia időbeni csökkenése 6
MECHANORECEPTOR Érzet intenzitása kis érzékenység fAP VRP nagy érzékenység I-Io HIDEGRECEPTOR Érzet intenzitása fAP VRP azonos érzékenység I-Io NOCICEPTOR nagy érzékenység Érzet Érzet intenzitása intenzitása ffAP AP log VRP VRP kis érzékenység I-Io 5. ábra Különféle receptorokat érő adekvát ingerintenzitás, I-Io, a receptorpotenciál, a receptor primer afferensének akciós potenciál frekvenciája, fAP, és a szenzoros központban kialakuló érzet erőssége közötti összefüggés (lásd Steven-féle hatványfüggvény). A receptor érzékenysége az egyes intenzitás tartományokban a hatványkitevő, n, értékétől függ. 7 nem jelentős, akkor lassú az adaptáció (tónusos vagy statikus receptorok) (6. ábra) Lassan és gyorsan adaptálódó mechanoreceptorok együttesen teszik lehetővé, hogy a bőrt érő mechanikai behatást a maga komplexitásában érzékelhessük (7. ábra) Az ingerrel kiváltott érzet időtartama
a receptor és a receptor által kialakított jel feldolgozását végző központ(ok) adaptációjától függ. Az inger (jel) kódolása Az ingerben rejlő információ kódolása történhet: • • • intenzitás szerint (frekvenciakódolás) lokalizáció szerint (kollaterális gátlás) ingerfajta szerint (jelölt pályák, modalitások és szubmodalitások) Intenzitás szerinti kódolás: Az intenzitás szerinti kódolás alapját a Steven-féle összefüggés képezi. Az eredeti információt a RP közvetítésével kiváltott AP-sorozat frekvenciája hordozza, mely a primer afferens roston terjed a központi idegrendszer irányába. A receptorban történő elsődleges kódolás technikai értelemben egy ún analóg/digitális jelátalakítás (A/D konverzió), melynek során egy adott tartományban bármely értéket felvevő receptor-potenciálból (analóg jel) kialakul egy adott frekvenciájú AP-sorozat (digitális jel). Az AP-sorozat digitális jel, mert a
frekvencia egy maximális értékkel behatárolt tartományában nem vehet fel akármilyen tetszőleges értéket, hanem csak meghatározott (diszkrét) értékeket. A kódolásra alkalmas digitális frekvenciaskála felbontását az adott receptorra és afferentációjára jellemző akciós potenciálok paraméterei, a vezetési sebesség és az ingerület szinaptikus átkapcsolásának folyamatai együttesen határozzák meg. A RP elektrotónusos tulajdonságai miatt csak helyi válasz kialakítására alkalmas, hosszabb távon amplitúdója folyamatosan és jelentősen csökken, ezért információ továbbítására nem alkalmas. Az AP viszont terjedése közben hosszabb távon sem veszít amplitúdójából, mivel terjedését az idegrost aktív membránfolyamatai (Hodgkinciklus) biztosítják. Az információ kódolásában az A/D jelátalakításnak tehát előnye az, hogy egy lokális, analóg jelből (RP), az információtartalom megőrzését biztosító, jelentős
távolságú továbbításra alkalmas új kód (frekvenciakód) születik. Ez a kód 8 INGER 6. ábra Lassan adaptálódó receptor primer afferensén az akciós potenciálok frekvenciája folyamatos ingerlés esetén időben csak kis mértékben csökken, míg a gyorsan adaptálódó receptor esetében egy-két akciós potenciál kialakulása után megszűnik a receptorválasz. Lassan adaptálódó (statikus), pl. ín-, izomorsó 100 % Gyorsan adaptálódó (dinamikus), pl. Pacini-test fAP 0% IDŐ POZÍCIÓ Adaptáció SEBESSÉG GYORSULÁS INGER 7. ábra Statikus és dinamikus mechanoreceptorok együttesen teszik lehetővé, hogy a bőrt érő mechanikai ingert a maga komplexitásában érzékelhessük. (Berne and Levy, Physiology, Fourth Edition, Fig. 7-4 alapján.) IDŐ Jelkonverzió D/A Receptor A/D D/A A/D D/A A/D A/D A Kód A D A D A D A D 8. ábra Analóg (A) és digitális (D) kód váltakozása a szenzoros információ neuronról neuronra
történő terjedésekor. A jel terjedése digitális, feldolgozása analóg formában történik 9 nem érzékeny sem az elektromos zajra, sem pedig az egymás mellett futó idegrostokon történő „adatforgalomra”. A kódolás lényeges eleme, hogy az A/D jelátalakítás a receptortól a felsőbb idegrendszeri központokig a szinaptikus átkapcsolódással kapcsolatban többször ismétlődik (8. ábra) Egy-egy szinapszishoz érkezvén ugyanis az AP-sorozat hatására a preszinaptikus membránon mediátor molekulák jutnak a szinaptikus résbe (mennyiségük az AP-sorozat frekvenciájának függvénye), majd diffundálnak a posztszinaptikus membránhoz, ahol egy újabb helyi, analóg választ váltanak ki (posztszinaptikus potenciál, D/A konverzió). Ez utóbbi az AP kialakítására képes membránrészre terjedve AP-sorozatot vált ki (A/D konverzió), melynek frekvenciája megegyezik a preszinaptikus AP-sorozat frekvenciájával. Ilyen módon az adekvát ingerre
vonatkozó, a receptorban kódolt információ ismételt A/D és D/A konverziók révén jut az afferens pályán a felsőbb központokhoz. A lokalizáció szerinti kódolás: Minden receptor, annak primer afferense, valamint további posztszinaptikus kapcsolatai receptív mezővel jellemezhetők (9. ábra) A receptív mező a térnek az a része, amelyből származó küszöb feletti adekvát ingerek a receptorban ingerületi folyamatot váltanak ki. A receptív mező a kontakt receptorokat körülvevő tér (tapintási receptorok), míg a telereceptorok esetében ez a térnek egy a receptortól távol eső része (fotoreceptorok). A térben elosztott receptorok (pl a bőrben lévő tapintási receptorok, vagy a retinában elhelyezkedő fotoreceptorok) valamelyikét érő inger helyét azáltal tudjuk meghatározni, hogy a receptorok térbeli elhelyezkedése, és a belőlük kiinduló ingerületi folyamatnak az agykérgi feldolgozóközpontokba történő vetülése (projekciója)
bizonyos szabályszerűséget követve megfelel egymásnak. Az ingerületi folyamat terjedésének, és a jelátkapcsolás valamint -feldolgozás térbeli organizációjának az ingerelt receptorok tényleges térbeli helyzetéhez való viszonyát a topológia jellemzi. A topológia akkor megtartott, ha az átkapcsolódási pontokon (szinapszisok) a párhuzamosan futó preszinaptikus rostok nem kapcsolódnak azonos posztszinaptikus neuronra. Az egymás mellett futó pre- és posztszinaptikus axonok ugyanakkor serkentő és gátló kollaterálisaikon keresztül egymással előre- illetve visszacsatolt kapcsolatot létesítenek (pl. kollaterális vagy széli gátlás), melynek alapján lehetséges az egymáshoz térben igen közeli ingerek elkülönítése (térbeli diszkrimináció). A kollaterális gátlás úgy növeli meg a térbeli diszkriminációt (csökkenti le a posztszinaptikus receptív mezők méretét), hogy két 10 + + 9. ábra Divergencia, konvergencia. A receptív
mező akkor megtartott, ha a szenzoros információ legfeljebb csak elágazódik (divergencia), de a posztszinaptikus neuronra más neuron nem szinaptizál (konvergencia). Egy posztszinaptikus neuron egyesíti a rá konvergáló preszinaptikus neuronok receptív mezőjét (középen). 10. ábra Kollaterális gátlás. Két egymáshoz térben közeleső inger egyidejű alkalmazásakor az egymást átfedő receptív mezők miatt a primer vagy szekunder afferensek frekvenciája alapján a két inger biztosan nem különíthető el egymástól. A meglévő kismérvű különbség a gátló jellegű kollaterális kapcsolatok miatt azonban posztszinaptikusan megnő. Ez a mechanizmus kiemeli a jel kontrasztját és így megkönnyti az ingerületi mintázat valósághű feldolgozását. 11 egymáshoz térben közeli inger esetén, az ingermaximumok közé eső receptív mezőből gátolja a posztszinaptikus afferentációt (10. ábra) Az inger fajtája szerinti kódolás: Az
ingerfajtára jellemző érzet kialakulását a receptor–pálya–központ együttesen határozza meg. A kódolás módja történhet az alábbiak szerint. • Jelölt pályák (alapvető modalitások, és szubmodalitások) • Mintázatok (ízérzés – térbeli, hőérzés – időbeli) • Tulajdonság detektorok (látás) Modalitáson az inger által keltett érzet minőségét, jellegét értjük. Az alapvető modalitások kódolása ún. jelölt pályákkal történik (pályán itt a receptor–pálya– központ együttest kell értenünk). A jelölt pálya bármely elemének (elektromos) ingerlése mindig azonos, a pálya által kódolt érzet kialakulására vezet. Ebből adódik, hogy a jelölt pálya érzet kialakulását akkor is lehetővé teszi, ha az nem párosul tényleges inger jelenlétével (hallucináció). Ezt a kódolási formát általában jól meghatározható topológia jellemzi. Jóval összetettebb érzet kialakulását teszi lehetővé az időbeli
és térbeli mintázatok alapján való kódolás. Az időbeli mintázatokkal történő kódolás esetében egy neuron többféle információt is továbbíthat aszerint, hogy a jelek időbeli mintázata milyen. A hidegreceptorok afferensein például 30 oC alatt csak spontán kisülés, míg 30 oC felett a hőmérséklet emelkedésével változó jellegű csoportos kisülések (burst) jelennek meg – ezzel, és nem az átlagos kisülési frekvenciával kódolva a hőmérséklet változását. A térbeli mintázatokkal történő kódolásra példa az ízérzés. A keserű és sós íz érzetét egy hármas neuronpopuláció ingerülete hozza létre. Keserű ízt akkor érzünk, ha mindhárom, sósat, pedig ha a háromból csak kettő kerül ingerületbe. A szenzoros kódolás kifinomultabb mechanizmusait a tulajdonság-detektorokban integrált neuronok működése hozza létre. Ezek az agykéregben található neuroncsoportok, melyek akkor kerülnek ingerületi állapotba, ha
összetett szenzoros bemeneti kapcsolataikon egy bizonyos komplex ingeregyüttes jelenik meg (pl. taktilis, optikai vagy akusztikus mintázatok észlelése). 12 A BŐR SZENZOROS FUNKCIÓJA A bőr testünk felületét teljes mértékben beborítja, így a külső környezetből származó ingerek első sorban a bőrt érik. A bőrt megközelítőleg egymillió idegrost innerválja Legnagyobb részük a durva mechanikus érzékelésben játszik szerepet. Egy kicsiny, de annál fontosabb részük kódolja az alábbi finom taktilis és egyéb modalitásokat: • finom mechanikus ingerek (tapintás, vibráció, nyomás) • hőingerek (hideg, meleg) • károsító, nociceptív ingerek (fájdalom) A mechanikus ingerek érzékelését gyorsan, és lassan adaptálódó mechanoreceptorok végzik. Felépítésük, működésük valamint a bőrben történő elhelyezkedésük alapján képesek a mechanikai ingerek sokaságából az alábbi szubmodalitások kiválasztására
és kódolására. I. Táblázat Receptor Receptív mező Adaptáció Kódolt szubmodalitás Pacini-testek nagy nagyon gyors vibráció Meissner-féle testecskék kicsi gyors sebesség Merkel-féle tapintókorongok kicsi lassú lokalizáció Ruffini-testek nagy lassú időtartam és intenzitás (Gyorsan adaptálódó mechanoreceptor a szőrtüszőreceptor is.) A 6. ábrán láttuk, hogy a Pacini-test folyamatos mechanikus ingerlés ellenére igen gyorsan beszünteti ingerület-leadását, tehát adaptációja nagyon gyors. Ennek egyik oka az, hogy a receptor centrumában található csupasz, ingerlékeny idegvégződést hagymalevélszerűen egy viszonylag nagyméretű burok borítja (11/A ábra). Ha a receptort nem túl hirtelen alkalmazott, folyamatos jellegű mechanikai inger éri, akkor az energia nagy része a lemezek egymáson történő elmozdítására fordítódik, így elegendő intenzitású mechanikai energia az idegvégződést nem éri, ezért azon
sem receptorpotenciál, sem akciós potenciál sorozat nem alakulhat ki (11/B ábra). Ha viszont a receptorral a mechanikai 13 ingert kellő intenzitásban és A Lamellált burok Idegvégződés Ingerlési mintázat B A lamellák átrendeződésére van kellő idő, így inger nem éri az idegvégződést Nincs afferens ingerület C A lemellák átrendeződésére idő nincs, így a jelentős lokális lamelláris deformáció az inger energiáját közvetíti a receptor membránjához Van afferens ingerület 11. ábra Egy gyorsan adaptálódó (dinamikus, fázikus) mechanoreceptor (A) válasza nem túlságosan hirtelen elkezdett és folyamatosan fenntartott (B) valamint rövid idejű és gyakran ismétlődő (C) mechanikai ingerlésre (vibráció) 14 kellően gyorsan közöljük, a lemezek a hirtelen energiabehatásra lokálisan deformálódnak, így mintegy utat engednek az energia terjedésének egészen az idegvégződésig, ahol a membrán deformációja
receptorpotenciál és következményes akciós potenciál sorozat kialakulását eredményezi (11/C és 12. ábra) Mindeközben a lemezek globális pozíciója nem változik jelentősen, mivel az átrendeződésre a gyors dinamika miatt nincs lehetőség. A Pacini-test receptív mezője nagy, mert a vibrációs energia terjedése a bőr szövetében nem okoz jelentős átrendeződést, és így a receptort távolabbról is érik vibrációs hatások. A Meissner-féle testecskék tokja jóval kisebb, és ezért csak közvetlenül a receptor feletti bőrrészlet ingerlése vezet AP-leadásra. A receptor csak akkor válaszol, ha az inger időben folyamatosan változik (12. ábra), ami például ujjainknak egy érdes felületen történő futtatásakor fordul elő. Érzékelésre valójában a mechanikai inger sebessége kerül (7. ábra) A Merkel-féle tapintókorongok speciálisak abban a tekintetben, hogy a tulajdonképpeni receptor nem az idegvégződés, hanem azok az
epiteliális sejtek, melyek a tapintókorongot alkotják. Ezek a sejtek szinaptizálnak a receptort innerváló idegrosttal. A receptor lassú adaptációja, felületes elhelyezkedése (13 ábra) és kis receptív mezője alkalmassá teszi a mechanikus inger (a bőr megnyomása) lokalizációjának kódolására. A Ruffini-testek folyadékkal teli kollagén tokkal körülvett idegvégződésből állnak: a tokot az idegvégződéshez (befelé) és a bőrhöz (kifelé) kollagén kötegek rögzítik. A nagy receptív mező és lassú adaptáció alkalmassá teszi a bőrt érő folyamatos mechanikai behatás (a bőr deformációja, elmozdulása, gyűrődése) mértékének kódolására mindaddig, míg az ingerhatás tart. A mechanoreceptorok bőrben való elhelyezkedése a természet logikáját követi, mely szerint a finom taktilis információt közvetítő Meissner-féle testecskék, Merkel-féle tapintókorongok és a szőrtüszőreceptorok a bőrben a lehető legfelületesebben
helyezkednek el, míg a vibrációt kódoló Pacini-testek a mélyebb rétegekben találhatók (13. ábra) 15 INGERLÉSI FORMA AFFERENS AP-SOROZAT log fAP log A bőrre ható nyomás intenzitása log A bőrre ható nyomás által előidézett deformáció sebessége log A mechanikai deformáció gyorsulása, mely azonos a vibráció frekvenciájával 12. ábra A bőrt érő mechanikus ingerek érzékelésének formái. A különféle mechanoreceptorok a mechanikai inger egy-egy jellemző tulajdonságára érzékenyek. Ezért az inger által keltett jelek feldolgozása már receptorszinten elkezdődik. A feldolgozás az agykérgi szinten fejeződik be és alakul ki a mechanikai inger által keltett érzet a maga komplexitásában. (SilbernaglDespopoulos, SH atlasz Élettan, 1994, 288. oldal B ábra alapján) SZŐRÖS BŐR SZŐRTELEN BŐR SZARURÉTEG Tapintás Tapintás Érintés FELHÁM Érintés IRHA KÖTŐSZÖVET Vibráció Merkel-sejt és -korong Meissner-féle
testecske Pacini-test Szőrtüsző receptor 13. ábra A bőr mechanoreceptorainak eloszlása. A bőrben az érintésre és nyomásra érzékeny receptorok felületesen, a vibrációra érzékenyek mélyebben helyezkednek el. (SilbernaglDespopoulos, SH atlasz Élettan, 1994, 288 oldal A ábra alapján) 16 Lassan és gyorsan adaptálódó mechanoreceptorok együttesen teszik lehetőve, hogy a bőrt érő mechanikai behatást a maga komplexitásában érzékelhessük (7. ábra) A hő érzékelését a bőrben két receptorféleség, a hideg- és melegreceptorok végzik. Ezek Aδ és C csoportba tartozó szabad idegvégződések, melyek AP-leadása statikus ingerlés esetén eltérő eloszlást mutat (14. ábra) Neutrális hőmérsékleti tartományban ezek a receptorok egyaránt spontán kisülést és teljes adaptációt mutatnak. Ezért kellemes hőmérsékleti körülmények között nem alakul ki bennünk egy folyamatos hőérzet. Ezeknek a receptoroknak a dinamikus válasza
egymás tükörképei: a hőmérséklet csökkenésére a hideg receptorok válasza átmenetileg nő, a melegeké átmenetileg csökken, a hőmérséklet emelkedésére pedig fordítva (15. ábra) A neutrális tartomány alatti hőmérsékletek kódolása a hidegreceptorok burst-szerű aktivitása alapján történik, mely a temporális mintázat alapján történő érzékelés egyik példája (16. ábra) Vegyük észre (14 ábra), hogy ebben a tartományban a hideg receptorok statikus hőingerre azonos kisülési frekvenciával válaszolnak, tehát a hőmérsékletet statikus aktivitásukkal nem kódolhatják! Hőérzetünket befolyásolja a megérintett tárgyak anyagi minősége is. Azonos hőmérsékletű fém- és fa tárgy közül a fémtárgyat hidegebbnek érezzük, mert a fémtárgy a bőrből több hőt von el, és így a hőreceptorok átlagosan alacsonyabb hőmérsékletre kerülnek valamint a megérintést követő hőtranziens is nagyobb (15. és 17 ábra) A bőr
hőmérséklete befolyásolja a hőérzetet azért is, mert – mint láttuk (15. ábra) – a hőreceptorok válasza a hőbehatásra tranziens jellegű, így a 35 oC-os hőmérsékletet hidegnek érezzük, ha bőrünk 40 oC-os, míg melegnek, ha az 30 oC-os. Hőérzetünk stabil hőhatás alatt a 18 ábrán feltüntetett módon a még károsodáshoz nem vezető hideg hőmérsékletektől (>0 o C) a már károsodáshoz vezető hőmérsékletekig (>45 oC) a hideg–neutrális–meleg– forró majd fájdalmas átmenetek szerint alakul. A 45–49 oC közötti tartományban a hideg- és fájdalomreceptorok leadása fokozódik, ezért a forró érzet kialakulása előtt paradox hideg- és fájdalomérzés jelentkezik. A szöveti károsodással járó ún. nociceptív ingereket szintén Aδ- és C-csoportba tartozó szabad idegvégződések veszik fel. Ezek ingerülete fájdalommal jár, mely 17 Melegreceptrok Neutrális tartomány Hidegreceptorok fAP 20 Paradox
hidegérzés 30 40 50 o C ÁLLANDÓSULT BŐRHŐMÉRSÉKLET 14. ábra A bőr thermoreceptorainak válasza állandósult bőrhőmérsékletű hőingerekre T = 33 oC Spontán kisülés! T = 30 oC HIDEGRECEPTOR MELEGRECEPTOR 15. ábra A bőr thermoreceptorainak válasza tranziens hőingerekre. (Bullock, Boyle III, Wang, NMS Physiology, Third Edition, Fig. 5-5 alapján) T = 34 oC ∆T ∆T = 4 oC ∆T = 6 oC 16. ábra Hőinger kódolása temporális mintázattal (hidegreceptorok burst-aktivitása) 18 30 oC FATÁRGY melegebbnek érezzük 30 oC FÉMTÁRGY hidegebbnek érezzük 17. ábra A hőérzet függ a megérintett tárgy anyagi minőségétől is. A bőrhőmérséklet eloszlását ú.n izotermikus vonalakkal jelöltük Mint látható, a fémtárgy nagyobb hőelvonása miatt a fémtárggyal érintkező bőr jobban lehűl, mint a fatárgy alatt. o C FÁJDALOM KÁROSODÁS 45 35 MELEG NEUTRÁLIS ADAPTÁCIÓ 32 HIDEG 18. ábra Az állandósult hőérzet és a
receptor funkcionális állapotai közötti kapcsolat 19 vitális jelentőségű, hiszen tudatosodás esetén felhívja az élőlény figyelmét a folyamatban lévő, szöveteit károsító folyamatra. A bőr nociceptorainak adekvát ingere pontosan nem ismert, de feltételezhető, hogy a fájdalmas stimulust a sejtek károsodásakor felszabadult kémiai anyagok, mint pl. hisztamin és bradykinin jelentik. A korábbi elképzelés – miszerint a kiváltott fájdalom a bőrben lévő mechano- vagy kemoreceptorok túlingerlésének volna köszönhető –, mára már tarthatatlanná vált. A károsító ágensek specifikus nociceptorok ingerületével váltják ki a fájdalmat. Ezeknek jellemzője, hogy szabad idegvégződések, és nincs jelátalakító burkuk (19. ábra) II. Táblázat Nociceptor Innerváló rost Specifikus Polimodális Aδ C kémiai termikus mechanikus Inger forró + K , serotonin, bradykinin, hisztamin hideg Mediáció glutamát glutamát
és P-anyag Vezetés gyors (12-30 m/s) lassú (0,5-2 m/s) lokalizált diffúz Lokalizáció Mint azt az 5. ábrán láthattuk, a nociceptorok ingerülete a károsító inger intenzitásával exponenciálisan nő, melynek oka ezen receptorok szenzitizációjában, az ingerbehatásra bekövetkező érzékenyülésében keresendő. Ennek egyik mechanizmusa a 19. ábrán látható A primer károsító inger sejtkárosodással jár, melynek folyamán az elhaló sejtből proteolítikus enzimek szabadulnak fel, melyek a keringő γ-globulinokból bradykinint hasítanak le. A bradykinin-molekulák a szabad nonciceptív idegvégződés membránjához kötődve másodlagos hírvivő mechanizmuson keresztül az idegvégződést érzékenyebbé teszik. A sejtkárosodási folyamat előrehaladtával ez a folyamat önerősítő jelleggel folytatódik (circulus vitiosus), mely magyarázza a nociceptív ingerület-leadás exponenciális fokozódását és azt, hogy kismértékű
ingerintenzitás növekedés a fájdalom jelentős fokozódásával jár. 20 A szenzitizációnak egyéb mechanizmusai is vannak, melyek mediátorai különféle anyagok lehetnek (K+, szerotonin, prosztaglandinok). Régóta megfigyelt jelenség, hogy a bőrt érő különféle károsító behatás bőrpírral, a bőr duzzanatával, a bőr hőmérséklet lokális emelkedésével, valamint fájdalmasságával jár. Ezeket a tüneteket a klinikumban rubor, tumor, calor és dolor latin szavakkal jelöli. Kialakulásuk mechanizmusát sematikusan a 20. ábra szemlélteti A károsító inger által keltett primer ingerületi folyamat az ingerlés helyétől antidrómos irányban terjed a szomszédos szabad idegvégződésekhez (axon reflex), ahol P-anyag és calcitonin gene-related peptide (CGRP) felszabadulását idézi elő. Ezek az anyagok a helyi környezet megváltozását okozzák, egyrészt azzal, hogy az erek falához diffundálva dilatálják azokat. Ennek eredménye a bőrpír
(rubor) és a fokozott véráramlás miatti bőrhőmérséklet-emelkedés (calor). Ezek az anyagok megnövelik az érfal (kapilláris, venula) permeabilitását, és így fokozzák a filtráció irányú Starling-erőket azáltal, hogy előidézik a plazmafehérjék extravazációját, ami fokozza az interstícium kolloid ozmotikus nyomását. Ennek eredménye a interstíciumban a szabadvíz felszaporodása, az ödéma (tumor). 21 Bőr Noxa bradykinin Nociceptív idegrost γ-globulinok Proteolítikus enzimek Nociceptív transducer Elhaló sejt 19. ábra A bőr nociceptorok szenzitizációjának egyik mechanizmusa. (Berne and Levy, Physiology, Fourth Edition, Fig. 8-5A alapján) Mikrocirkulációs érhálózat Noxa Bőr Nociceptív idegrost 2. P-anyag felszabadulás Nociceptív terminál 1. Akciós potenciál antidrómos érkezése 4. Plazma extravazáció 3. Fokozott mikrorcirkulációs áramlás és permeabilitás 20. ábra A bőrt érő nociceptív behatás által
kiváltott klinikai tünetek („color, rubor, dolor, calor”) kialakulásának mechanizmusa. (Berne and Levy, Physiology, Fourth Edition, Fig 8-5B alapján.) 22 SZOMATOSZENZOROS AFFERENTÁCIÓ A receptorok által felvett ingerek a periférián a receptorokat innerváló primer neuronon frekvencia kódban jelennek meg. A kódolt jel centrifugális irányban terjed a jelfeldolgozást végző központok felé. Egy idegrost csakis egy modalitást közvetít Az idegrostok átmérője, vezetési sebessége és az általuk innervált receptor modalitása szoros és logikus funkcionális kapcsolatban állnak (III. Táblázat ) III. Táblázat (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-6 alapján) Myelin-hüvely Myelinizált nélküli Rostátmérő (mikrométer) 20 15 10 5 1 2 0.5 6 2 0.5 Vezetési sebesség (m/s) 120 90 60 30 ÁLTALÁNOS OSZTÁLYOZÁS A C α β γ δ Izomorsó (primer) Izomorsó (szekunder) Szőrtüszőreceptor Vibráció
(Pacini-test) Finom tapintás (Meissner-féle testecskék) Durva tapintás/nyomás Mély nyomás és tapintás Akut fájdalom Krónikus fájdalom Hidegérzés Melegérzés HÁTSÓ KÖTEGLEMNISCUS MEDIALIS RENDSZER ANTEROLATERÁLIS RENDSZER 23 A gerincvelő hátsó szarva, mint a primer afferentáció átkapcsolódási helye A központi idegrendszeri projekció során a jel a szinapszisokban többször átkapcsolódik, tehát egy afferens pálya több neuronból áll (elsődleges, másodlagos, harmadlagos stb. neuronok) Az átkapcsolódásra az első lehetőség a gerincvelő hátsó szarvában van (21. ábra), melynek szerkezete lamináris (Rexed-laminák) Egy-egy laminában általában azonos típusú rostok szinaptizálnak (Aδ, C, Aβ, stb.) Minden átkapcsolódás egyben a jel által kódolt információ feldolgozására ad lehetőséget azáltal, hogy a jel digitális formából (frekvenciakód) a posztszinaptikus membránon analóg formára vált. Az analóg jelek
(EPSP-k vagy IPSP-k) a posztszinaptikus membránon az elektrotónusos feszültségek szabályszerűségei szerint integrálódnak, és így nagy gyorsasággal kialakul az az eredő, kimeneti jel, mely ismét digitális formában terjed tovább a következő szinapszisig. Egy neuron elágazó axonterminálisai számos kapcsolatot létesítenek a posztszinaptikus sejtekkel Ezek között vannak olyan sejtek is – az interneuronok –, melyek nem az aszcendáló kapcsolat elemét képezik (tehát nem szekunder vagy tercier neuronok), hanem kollaterális kapcsolatot teremtenek az aszcendáló pálya neuronjai és az adott átkapcsolódási környezet egyéb neuronjai között. Az interneuronok által kialakuló kapcsolat lehet serkentő vagy gátló jellegű, előre- vagy visszairányuló (rekurrens). Ezek a sejtek a szenzoros információ alacsonyrendű feldolgozásának elemei, melyek modalitásspecificitást mutatnak. A gerincvelő hátsó szarvának neurokémiája igen változatos,
mediátorai között szerepelnek a katecholaminok, aminosavak, szomatosztatin, Panyag, endogén opiátok stb. Aδ 21. ábra A gerincvelő hátsó szarvának lamináris szerkezete (Rexedlaminák). Ezekben a rétegekben találhatók egyes receptorok (hő, fájdalom, durva tapintás) másodlagos afferensei illetve nagyszámú interneuron, melyek a gerincvelői szenzoros jelfeldolgozás fontos elemei. C Aβ 24 Feldolgozási lehetőségek az afferens jel központi idegrendszeri átkapcsolódásai során Egy-egy roston belül az adott modalitású jel különböző intenzitásainak továbbítására kétféle lehetőség van. Ha az egyre erősebb inger egyre több receptív mezőt hoz ingerületbe, és így a roston belül egyre több neuron, illetve annak axonja kerül ingerületbe (22. ábra), térbeli szummációról beszélünk A másik lehetőség az időbeli szummáción alapul, amikor is az inger intenzitásával arányosan változik egy adott axon kisülési frekvenciája. A
szinaptikus áttevődés a jelfeldolgozás egyik alapvető lehetősége, mert a szinaptikus válasz kialakítása az analóg posztszinaptikus potenciálok integrálása révén történik. A feldolgozás komplexitását növeli, ha a jelfeldolgozásban több neuron vesz részt. Valóban, a központi idegrendszer különböző részein a neuronok anatómiai és egyben funkcionálisan szervezett csoportokat (pool) alkotnak. Ezek bemenetét igen gazdag elágazódási mintázatot mutató axonok alkotják. Egy erősen leegyszerűsített példát látunk a 23. ábrán A pool-ba belépő afferensek (B1 és B2) a valóságban ezres nagyságrendben finom terminális rostokra oszlanak, melyek gazdagon szinaptizálnak a pool neuronjainak dendritjein és somáján. A dendritek a valóságban szintén dúsan arborizáltak, így jelentősen megnövelve a bejövő szinaptikus kapcsolatok számára a kapcsolódási felületet. Az afferens kapcsolatok ily módon innervációs mezőket alkotnak. Vannak
a pool-ban olyan neuronok, melyek egy-egy afferens innervációs mezőjének középpontjában helyezkednek el, vannak olyan sejtek is, melyekkel több afferens is szinaptizál (a K3-kimenetet adó sejt) és vannak olyanok is, melyek egy adott afferenshez viszonyítva periférikus helyzetűek, rajtuk csak kis számú szinapszis található (a K1-kimenetet adó sejt). Egyetlen preszinaptikus akciós potenciál (AP) egyetlen szinaptikus kapcsolatban nem vált ki posztszinaptikus AP-t, csak EPSP-t vagy IPSP-t. A preszinaptikus rostok arborizációja biztosítja, hogy ez megtörténhessen, tehát a beérkező jel szinaptikus átkapcsolódása biztosított legyen. Az ingerlési mezők középpontjában, illetve ezek átfedéseiben lévő sejtek egy beérkező AP hatására biztosan tüzelni fognak, hiszen kellő számú szinaptikus kapcsolat egyidejű (térbeli szummáció) vagy egymást időben gyorsan követő (időbeli 25 GYENGE INGER Receptív mezők Idegrost KÖZEPESEN
ERŐS INGER ERŐS INGER 22. ábra Jelintenzitás továbbítása térbeli szummációval 26 Idegrost keresztmetsze B1 K1 K2 K3 B2 K4 23. ábra Egy neuroncsoport (pool) viszonya a gazdagon elágazó afferens végződésekhez. Számos afferens végkészülék szinaptizál egyetlen neuronnal. Szummált posztszinaptikus potenciáljaik biztosítják, hogy az afferens ingerület biztosan továbbjusson a szinapszison. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-9 alapján) BEMENET KIMENETEK POOL Kisülési zóna Facilitált zóna 24. ábra A neuroncsoporton belüli ingerlékenységi szintek. A pool centrumában lévő sejtek elegendő számú afferens jelet kapnak ahhoz, hogy biztosan küszöb feletti, kisülési állapotba kerüljenek. A kisülési zónát körülvevő területen a neuronok ingerületi állapota facilitált, mert a beérkező afferentáció nem elégséges ugyan akciós potenciál kiváltásához, de már bizonyos mértékű
depolarizációt kivált – így érzékenyebbé téve a neuront a további afferens ingerületekre. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig 46-10 alapján.) 27 szummáció) ingerületi állapota biztosítja a posztszinaptikus membránterületek küszöböt meghaladó depolarizációját (24. ábra) A kisülési (discharge) zóna környékén található neuronok is részesednek az afferens szinaptikus kapcsolatból, de nem elegendő számban, vagy időben nem kellő gyakorisággal ahhoz, hogy arra AP-lal válaszoljanak. Az őket érő afferentáció hatására ezen sejtek nyugalmi állapota megszűnik, membránpotenciáljuk közelebb kerül a küszöbpotenciálhoz, tehát facilitált állapotba kerülnek. Ebben az állapotban már egyetlen küszöb alatti erősségű afferens jel is kiválthatja kimenetükön a választ. Ha az afferentáció gátló jellegű, akkor is érvényesül a fent leírt jelenség, azonban ellenkező előjellel. A pool-t
alkotó neuronpolpulációt érő serkentő és gátló befolyások tehát a pool-on belül térben és időben az ingerületi állapot bonyolult mintázatát eredményezik. Ezek a mintázatok a pool anatómiai és funkcionális organizációjának szabályai szerint alakítják a pool kimenetén a jelmintázatot. A neuronális polpuláció tagjai között alapvetően háromféle kapcsolat van. Az egyik lehetőség, amikor egy preszinaptikus neuron egy posztszinaptikus neuronnal szinaptizál (1:1 kapcsolat). A jelfeldolgozás szempontjából ebbe a kapcsolatba kollaterális facilitáció vagy gátlás révén lehet beavatkozni, melynek eredményeként a posztszinaptikus neuronon a jel továbbítása biztosított, vagy blokkolódik (lásd a széli gátlás jelenségét). Az ingerületi folyamat központi idegrendszeri terjedésében a jelfeldolgozás másik két lehetősége a divergencia (25. ábra) és a konvergencia (26 ábra). Divergens kapcsolatok funkcionális értelemben
erősítőként működnek, illetve lehetővé teszik, hogy az afferens információn több feldolgozó központ osztozzék (pl. a hátsó kötegben aszcendáló proprioceptív afferentáció leágazása a cerebelláris magvak felé). Egyetlen afferens elágazásaiból származó konvergens kapcsolatok (lásd fenn) biztosítják, hogy a posztszinaptikus neuron biztosan válaszoljon az afferens jelre (26/A ábra). A több forrásból érkező afferentáció (26/B ábra) különféle jelfeldolgozási művelet elvégzésére – mint integrálás, összehasonlítás, rendezés – nyújt lehetőséget. A konvergencia a posztszinaptikus neuron receptív mezőjének méretét növeli, illetve modalitását megváltoztathatja (unimodális–polimodális átalakulás). 28 25. ábra Divergens neuronhálózatok. Funkcionálisan erősítési, elosztási, szenzoros vagy motoros kópia készítési szerepük van. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-11
alapján) A B 26. ábra Konvergens neuronhálózatok. Funkcionálisan biztosítják a szinaptikus kapcsolat megbízhatóságát, és összegző (integráló), összahasonlító, rendező szerepük van. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-12 alapján) 29 A felszálló szomatoszenzoros rendszerek működése A különböző modalitások elkülönülten terjednek a nagy felszálló rendszerek rostjaiban. A legjelentősebbek a hátsó köteg–lemniscus medialis rendszer (HK–LM), és az anterolaterális rendszer (AL) (27. ábra) A trigeminalis rendszer a HK–LMrendszerrel analóg elven épül fel A hátsó köteg–lemniscus medialis rendszer: • A primer afferensek 20%-át tartalmazza • Modalitások: diszkriminatív tapintás, kinesztézia, propriocepció (lásd a III. táblázatot) • Gyorsan vezető rostok (lásd a III. táblázatot) • Szigorú szomatotópia • A rostok modalitás specifikusak vagy polimodálisak •
Átkapcsolódás a hátsókötegi magvakban • Másodlagos neuron: a hátsókötegi magvakból a lemniscus medialis-szal projiciál a thalamusba • Másodlagos projekció a thalamus VPL magjába • A rendszer NEM tartalmaz nociceptív rostokat A HK-magvak (ncl. gracilis et cuneatus) átkapcsoló (relay) sejtjei glutamát, míg a preszinaptikus gátló sejtek GABA-mediációval működnek. A HK–LM-rendszerben reprezentált taktilis modalitások között nem szerepel a durva tapintás, ez ugyanis az AL-rendszerhez tartozó tr. spinthalamicuson keresztül aszcendál (28. ábra) A taktilis információ kétszeres reprezentációja miatt csak a gerincvelő kiterjedt sérülései járnak súlyos taktilis deficittel. A HK–LM-rendszer által továbbított taktilis információ finom tapintásra, nyomásra, alacsony (lebegés vagy „flutter”) és magas frekvenciájú vibrációra épülő részletes analízist tesz lehetővé, melynek nagy a gnosztikus értéke. A
propriocepció vagy sajátérzékelés lehetővé teszi, hogy tudatos vagy reflex-szintű információnk legyen ízületeink helyzetéről, izmaink tónusáról, általuk megvalósuló mozgások dinamizmusáról (kinesztézia), és testünk helyzetéről (29. ábra) Ezekhez a funkciókhoz természetesen gyorsan vezető rostok által megteremtett afferens kapcsolatok szükségesek (III. Táblázat) A rendszert szigorú szomatotópia jellemzi. Az alacsonyabb gerincvelői szinten belépő afferenseket a felsőbb szinteken belépők mediális irányba szorítják, ezért a hátsó 30 kötegben a topológiai viszonyokat tükröző ú.n szenzoros homunculus helyzete lábbal a középvonal irányába mutat, a HK-magvakkal felépülése a nyakkal zárul. Fejét majd HÁTSÓ KÖTEG LEMNISCUS MEDIALIS RENDSZER ANTEROLATERALIS RENDSZER Leminscus medialis Tr. spinothalamicus ventralis 27. ábra A gerincvelő két legfontosabb aszcendáló rendszere, a hátsó köteglemniscus medialis és
az anterolateralis rendszer. Figyeljük, meg, hogy a HK–LM-rendszer átkapcsolódás nélkül, míg az AL-rendszer hátsószarvi átkapcsolódás és zömmel az ellenoldalra történő átlépés után kezdi meg felszállását a felsőbb központok felé. Ezért a HK–LM-rendszerben a felszálló ág primer, míg az AL-rendszerben szekunder neuron. Hátsó köteg magvak Finom lokalizációjú diszkriminatív tapintás, kinesztézia (tér- és időbeli mintázat) Durva lokalizációjú tapintás 28. ábra A hátsó köteglemniscus medialis rendszer és az általa közvetített modalitások (tapintás/nyomás, „lebegés”/vibráció). Figyeljük, meg, hogy tapintási információ (durva) az AL-rendszerben is reprezentált, így csak nagyon kiterjed gerincvelői sérülés esetén van teljes taktilis kiesés 31 Agykéreg Cerebellum Thalamus ATAXIA: A kisagy proprioceptív Hátsó köteg bemenete hiányzik Hátsó köteg Anterolaterális köteg magvak Receptorok:
izomorsó inorsó bőr mechanoreceptorok 29. ábra A hátsó köteglemniscus medialis rendszer és az általa közvetített modalitások (propriocepció). A felszálló kapcsolatok a propriocepció gnosztikus feldolgozását szolgálja, míg a szegmentális és interszegmentális kapcsolatok a reflexes mozgáskoordináció szolgálatában állnak 32 a thalamus-ban „kapja meg”, ahol a trigeminális rendszer által összegyűjtött szenzoros információ egyesül a HK–LM- rendszer területéről származó afferentációval. A HK–LM-rendszerben aszcendáló jelek thalamikus átkapcsolódását precíz szomatotópia jellemzi. A fej területéről származó információ dominánsan a VPM thalami-ba, míg a test egyéb területeiről a VPL thalami-ba vetülnek a n. trigeminus illetve a lemniscus medialis szekunder afferensei. A legkaudálisabb területek a VPL thalami laterális részébe, a váll és kéz a VPL thalami mediális részébe, a kéz proximális része a VPM
thalami laterális részébe, míg a fej a VPM thalamiba, a száj körüli részek és a száj nyálkahártyája a VMP thalami legmediálisabb területére vetül. A thalamikus neuronok receptív mezője kisméretű, vagy a primer vagy a szekunder neuronénak felel meg és a rendszer kereszteződése miatt az ellenoldali testfélre lokalizáltak. A HK–LM-rendszer jeleinek kérgi projekciója és feldolgozása a thalamus VPL és VPM specifikus magjaiból az agykéreg primer szenzoros areájába (SI) történik oly módon, hogy a thalamus szintjéig megtartott szomatotópia megmarad, és egyben a reprezentált modalitásoknak megfelelően megnégyszereződik. A szigorú szomatotópia ellenére az agykérgi működés plaszticitást mutat, sérülés esetén képes a funkciók bizonyos mértékű átrendezésére, a kiesett funkciók helyettesítésére. Az SI kérget négy Brodmann-area alkotja (30. ábra), melyben az egyes modalitások dominanciája különböző: 3a –
izomorsó afferensek, 3b – tapintás, 1 – gyorsan adaptálódó felületes receptorok, 2 – izületekre bontott mélyérzés. A feldolgozás a 3a– 3b–1–2 sorrendben egyre komplexebb. Mindegyik Brodmann-areának saját homunculusa van. A kérgi szenzoros homunculus arányai tükrözik azt a sejtarányt, melyet az adott kérgi szenzoros area neuronális pool-ja az ellenoldali megfelelő testtájból származó szenzoros információ feldolgozásának szentel. Ez az arány igen nagy a száj és környékére vonatkozóan, a kéz ujjainak megfelelően, de például igen alacsony a hátnak megfelelően. Vegyük észre, hogy a thalamikus specifikus projekció nem csak a homunculus-szal jellemezhető térbeli elrendeződést mutatja, hanem egy bőr (felületi – taktilis) és izom (mély – prorioceptív) irányút is, mely szerint a thalamus kérgi részébe vetült izmokból és ízületekből származó proprioceptív és mélyérzési afferentáció az SI perifériájára
(Br. 3a és 2), míg a thalamus magjába vetült bőrből származó taktilis afferentáció az SI centrumába (Br. 3b és 1) jut 33 PRIMER MOTOROS AREA PRIMER SZENZOROS AREA 1 4 2 izületekre bontott mélyérzés 3b 3a Köpeny (izomokból, ízületekből ⇒ propriocepció) A kézizomzat szenzoros és motoros innervációja szorosan integrált izomafferensek THALAMUS Mag (bőrből ⇒ taktilis érzékelés) 30. ábra A hátsó köteg – lemniscus medialis rendszer által közvetített modalitások thalamocorticalis projekciója a primer szenzoros areába. A szenzoros homunculusszal jellemzett topológia mellett nagymértékű funkcionalitás jellemzi a projekció topológiáját. Pl a kéz izomzatának szenzoros (Br 3a) és motoros (Br 4) innervációja szomszédos területekre lokalizált. (Berne and Levy, Physiology, Fourth Edition, Fig 8-12 alapján.) Modalitás X Modalitás Y Gátló udvar Modalitás Z 0,5 mm 31. ábra Az agykérgi szenzoros jelfeldolgozás
kolumnáris organizációja. Vázlatosan három kolumna látható az agykéreg felszínére vetítve. A kolumnák modalitás-specifikusak Központjukat gátló udvar veszi körül. 34 (30. ábra) A primer areát egy másodlagos, még összetettebb feldolgozást végző terület (SII) határolja. Az agykérgi jelfeldolgozást a kolumnáris organizáció jellemzi Ennek lényege, hogy kb. tízezer neuron az agy felszínére merőleges kb 0,5 mm átmérőjű oszlopokba rendeződik, és egymással szoros kapcsolatot alakít ki egy szubmodalitás meghatározására, analízisére a test egy pontjára vonatkozóan. Az agy felszínét a nagyszámú kolumna mozaikszerűen borítja be. A kolumnák által analizált modalitások keverednek, így az egyes kolumnák közötti szomszédos kapcsolatok kialakításával egyre komplexebb analízisre nyílik lehetőség (31. ábra) Ezért a kolumnáris szerveződés alkalmas összetett tulajdonságok jelenlétének jelzésére
(tulajdonság-detektor, majomkísérletes példa: egy kolumna leadása akkor volt maximális, ha a tenyeret egy taktilis ingersorozat diagonális irányban, a csukló ulnáris részétől a mutatóujj tövének irányában érte). A specifikus thalamikus afferentáció a kolumna IV. rétegébe érkezik és a II, III, V és VI rétegekből lép ki a kolumnáris feldolgozás végeredményét képező jelsorozat, és halad a szomszédos vagy távolabbi kolumnák felé, ahol a feldolgozása már más szempontok szerint tovább folyatódik. Az SI régió funkcionális jellemzésére legmegfelelőbb, ha felsoroljuk, hogy milyen kiesésekkel kell számolnunk az SI-régió teljes pusztulásakor (vagy műtéti eltávolításakor). • A szomatotópia szerinti kiesések jellemzőek, de plaszticitás is van! • SII kiesése nincs hatással SI-re, mert sorbakapcsoltak. • A személy nem tudja lokalizálni a finom, diszkriminatív taktilis inger forrását. Meg tudja ugyanakkor határozni,
hogy mely végtagon, nagyobb testtájon történik az ingerlés, jelezve ezzel, hogy a szubkortikális központok bizonyos mértékű lokalizációra képesek. • A személy nem tudja meghatározni a bőrét ért nyomás mértékét. • A személy nem tudja meghatározni a tárgyak súlyát. • A személy nem tudja meghatározni a tárgyak alakját, formáját (stereognosis hiánya), illetve nem ismeri fel a bőrére írt betűket, jeleket (graphesthesia hiánya). • A személy nem tudja megítélni egy általa megérintett, végigsimított felület anyagi minőségét, ugyanis ehhez a finom taktilis ingereket közvetítő bőr mechanoreceptorokból származó jelek komplex kérgi feldolgozása szükséges. • Mivel a HK–LM-rendszerben a hő- és fájdalomérzet nem reprezentált, ezért a hő- és fájdalomérzet megtartott, de a személy nem tudja kritikusan értékelni és lokalizálni ezeket a modalitásokat. Az anterolaterális rendszer és a fájdalom
fiziológiája: 35 • Kizárólag posztszinaptikus rostok alkotják • Kontralaterálisan a VPL thalami-ba vetülnek • Bilaterálisan a formatio reticularis-ba vetülnek • Fő pályája a tr. spinothalamicus • Modalitások: nocicepció (fájdalom), hőérzés, durva tapintás • Rostjai lehetnek gyors vezetésűek és modalitásspecifikusak, vagy lassúak és polimodálisak • Nagyon sok a viszcerális impulzus (Head-zónák, szomatoviszcerális kapcsolatok) • NINCS specifikus agykérgi projekciója A tr. spinothalamicus sejtjei két csoportba sorolhatók Az egyik csoport ingerküszöbe alacsony, sokféle ingerre érzékenyek (polimodálisak, aspecifikusak) és válaszuk arányos az ingerintenzitással, annak széles tartományában (széles dinamikus tartományúak). Az aspecifikus sejteken sok mechano- és nociceptor konvergál A gyenge ingerrel kiváltott válaszukat a magasabb központok blokkolják. Ha ez nem következik be, akkor már enyhe
mechanikus ingerek is fájdalmat váltanak ki (mechanikus allodynia). A másik csoportot azok a sejtek alkotják, melyek ingerküszöbe magas, csak specifikus nociceptív ingerekre válaszolnak. Az anterolaterális rendszer által közvetített fájdalom biológiailag és így klinikailag is nagyon jelentős modalitás. A tr spinothalamicus kétféle rostkontingenst tartalmaz, mely az akut illetve a krónikus fájdalom közvetítéséért felelős (IV. Táblázat) IV. Táblázat A pálya neve Tr. Paleospinothalamicus Tr. Neospinothalamicus Vezetési sebesség lassú (C) gyors (Aδ) Modalitás specificitás polimodális specifikus Thalamikus projekció nem specifikus magvak specifikus magvak A thal. projekció jellege diffúz lokalizált Precíz kérgi lokalizácó nincs A fájdalom jellege késői, tompa, erős, diffúz Kiváltott reflexek antalgiás, kímélő tartás, vegetatív tünetek 36 lokalizáció és mennyiségi kiértékelés a kéregben korai, éles
menekülési reflexek A fájdalomérzet kialakulásához nem szükséges az agykéreg! Az agykéreg a fájdalmi információ diszkriminatív, értelmező feldolgozását végzi. A thalamus működése adja a fájdalom eredendően negatív emocionális töltését. Így érthető, hogy a thalamus sérülése (pl. agyvérzés) esetén az ellenkező testfélre lokalizált, rendkívül heves, kellemetlen jellegű, fájdalmas állapot kialakulását eredményezheti tényleges fájdalmas inger jelenléte nélkül (thalamus szindróma, centrális fájdalom). A frontális lebeny határozza meg, hogy a fájdalom mennyire kellemetlen, és hogy mennyire zavarja a beteget. Ezért, különösképpen a fájdalom gyógyszeres befolyásolhatóságának hiányában, korábban a prefrontális lobektómia hasznosnak bizonyult igen erős fájdalmak (pl. rákos betegség) csillapítására (A fájdalom sebészi csillapításának egy másik sebészi eljárása az anterolaterális cordotomia,
mikor is a tr. spinothalamicus lateralis rostjait vágják át, általában a ventrális tapintási információt közvetítő rostok épen hagyásával. Ha ezek mégis átvágásra kerülnének, taktilis kiesés mégsem tapasztalható, hiszen a HK–LM-rendszer intakt marad.) Viszcerális eredetű fájdalom gyakran sugárzik bőrfelszínünk tipikus régióiba. Ennek oka az, hogy a gerincvelő szegmentális elvet követve fejlődik, és emiatt úgy a szenzoros, mint a motoros innerváció szegmentális jellegű (Head-zónák). Egy szegmens által beidegzett bőrterületről (dermatóma) származó afferens rost, és az adott szegmens által innervált zsigeri terület afferentációja egyazon gerincvelői neuronra konvergál, és így a zsigeri eredetű fájdalom az adott dermatómára vonatkoztatva tudatosul. Egy másik lehetőség az, ha egy facilitált állapotban lévő szomatikus neuronnal szinaptizáló viszcerális kollaterális idézi elő a szomatikus neuron válaszát. A
sugárzó fájdalom klinikai jelentősége nagy, hiszen felhívja az orvos figyelmét a potenciálisan súlyos következményekkel járó viszcerális kórfolyamatra (pl. a szívizom csökkent véráramlásával járó állapotában fájdalom jelentkezhet a bal vállban és karban). Egy végtag elvesztése, vagy műtéti eltávolítása után – annak ellenére, hogy a sebgyógyulás és a szöveti regeneráció már befejeződött – fájdalmas inger hiányában is fájdalom jelentkezhet, melyet a beteg az elvesztett végtagba lokalizál (fantomfájdalom). Látható, hogy a fájdalom észlelése egy igen kiterjedt neurális rendszer integrált működéséhez kötött. Ha a rendszer egyes elemei kiesnek vagy kapcsolatukban zavar támad, az egy kóros természetű, adott esetben igen intenzív fájdalom kialakulásához vezethet, melynek csillapítása nagyon nehéz. 37 Intenzív fájdalommal járó állapotok működésbe hozzák az endogén analgetikus rendszert, mely
átmeneti időre a fájdalmat hatékonyan képes csökkenteni, és így lehetőséget ad a fájdalmas ingertől való eltávolodásra. A rendszer vertikálisan szervezett gátló neuronokból áll. Kiindulási helye a periaqueductalis magvak, és támadáspontja a fájdalmi ingerület gerincvelői színtű elsődleges átkapcsolódása (32. ábra). A rendszer endogén stimulánsai az endogén ópiátok (enkefalinok, endorphinok, dynorphin), melyek a µ, δ és κ ópiát receptorok természetes ligandjai. Az orvosi praxisban leggyakrabban használt természetes ópiát a morfium, egy igen erős kábítószer, melyhez azonban az endogén ópiátokkal szemben, gyakran alakul ki végzetes jellegű gyógyszerfüggőség. Használata súlyos, szenvedéssel járó esetekben elkerülhetetlen. Az endogén analgetikus rendszer működése a primer fájdalmi ingerület gerincvelői mediációjának pre- és posztszinaptikus gátlására irányul (33. ábra). A rendszert alkotó gátló neuronok
ingerületi állapota a rendszer inaktív és aktív állapotaiban a 34. ábra szerint változik A rendszer inaktív állapotában a GABAerg neuronok tónusos gátlás alatt tartják a leszálló analgetikus pályát. A pálya egymást követő gátló neuronjainak működése az aktív (+) – inaktív (-) funkcionális állapotok szerint ismétlődik. Ennek végeredményeként a gerincvelői szinten az opiát neuronok gátolt állapotba kerülnek, tehát nincs analgézia. Morfin vagy endogén opitátok a rendszert annak eredeténél és a gerincvelői szinten hozzák működésbe, az előbbi esetben a GABAerg neuronok aktivitásának felfüggesztésével, az utóbbiban a nociceptív átkapcsolódás pre- és posztszinaptikus gátlásával. Mindkét hatás analgéziát eredményez. Az endogén analgetikus rendszer hatékonyságát jól jellemzik a harctéri vagy trauma-helyzetekben leírt esetek, amikor a súlyos traumát szenvedett egyén addig nem érzett fájdalmat, míg a
fájdalmat előidéző veszélyhelyzet el nem múlt, azt meg nem szokta, vagy segítség nem érkezett. Ekkor ugyanis a fájdalom előidézte felfokozott idegrendszeri állapot (stress analgézia) – mely endogén opiátokat szabadít fel – csökken, és így a rendszer inaktív állapotba kerül. 38 MORFIN OPIOID GÁTLÓ NEURON Periaq. magvak GABAERG GÁTLÓ NEURON MONOAMINERG GÁTLÓ NEURON Medulla MORFIN Gerincvelő Gátló mechanizmus 32. ábra A fájdalom endogén szupresszióját végző analgetikus rendszer szerkezete. A rendszer vertikálisan kapcsolódó gátló neuronokból áll. A leszálló rendszer támadáspontja a nociceptív ingerületek első gerincvelői átkapcsolódása. A folyamat vagy endogén, vagy exogén opiát ligandokkal stimulálható. (Fonyó, Az orvosi élettan tankönyve, második kiadás, 37-6. ábra alapján) 39 Opioid gátló interneuron Morfin (alsó) Pre- posztszinaptikus gátlás 33. ábra A gerincvelői nociceptív
mechanizmusának sémája átkacsolódás GÁTLÓ NEURONOK ÁLLAPOTOK Aktív (gátol) pre- és RENDSZER INAKTÍV posztszinaptikus gátló RENDSZER AKTÍV Opiát 1 Blokkolt Monoaminerg 2 + Tónusos gátlás Nem blokkolt Monoaminerg 1 Tónusos gátlás GABAerg Inaktív (nem gátol) Opiát 2 Gerincvelői átkapcsolódás NINCS ANALGÉZIA ANALGÉZIA 34. ábra Az endogén analgetikus rendszer inaktív és aktív állapotát jellemző funkcionális kapcsolatok 40 HK–LM-RENDSZER ANTEROLATERALIS RENDSZER Szinoním elnevezések • Specifikus • Epikritikus • Gnosztikus Klinikai alapon Szinoním elnevezések • Nem specifikus • Protopátiás • Hő- és fájdalomérzés Gyors Vezetés Precíz Megtarott Kis receptív mezők ARAS Lassú Diffúz Nagyfokú konvergencia és divergencia Szomatotópia neo- 1:1 SPECIFIKUS ASSZOCIÁCIÓS MAGVAK (Mediális, középvonali, pulvinar, reticularis) INT paleo- THALAMUS SPECIFIKUS MAGVAK (VPL [törzs,
végtagok] VPM [arc, fej] VL [xlat kisagy, ncl. ruber]) NEM SPECIFIKUS (DIFFÚZ) MAGVAK INT INT ASP (Ventr. ant, intralaminaris, középvonali) ASP 1:1 ARAS INT ASP AGYKÉREG ALATTI RÉGIÓK AGYKÉREG SPECIFIKUS KÉRGI ZÓNÁK (Szomatoszenzoros, szomatomotoros, halló-, látó-, Br. 3,2,1 [törzs, végtagok,arc,fej] Br. 4,6 [xlat kisagy, ncl ruber]) ASSZOCIÁCIÓS KÉRGI ZÓNÁK (A primer zónákkal szomszédos területek) 35. ábra A szomatoszenzórium szerkezete és az alkotóelemek közötti kapcsolatrendszer. ARAS = Aszcendáló Retikuláris Aktiváló Szisztéma, INT = integráló kapcsolat, ASP = aspecifikus kapcsolat. 41 AGYI ELEKTROMOS TEVÉKENYSÉG Az agy működése elektromos tevékenységének regisztrálásával követhető. Tanulmányozása jelentős segítséget nyújtott az agyi szenzoros, motoros és mentális tevékenység jobb megértéséhez. Az elektromos tevékenységet regisztrálhatjuk a fejbőrre helyezett elektródokkal, vagy az agy
felszínén (field- vagy mező-potenciál) illetve intracelluláris elektródákkal (unit- vagy egység-potenciál). Az agykérgi kiváltott potenciálok Az agykéregbe érkező szenzoros jel az agykéreg felszínén átmeneti potenciálváltozást hoz létre, melyet a kérgi felszín alatti denritek posztszinaptikus potenciáljainak összegződése, és nem a beérkező szenzoros AP-ok hoznak létre. Izolált primer kiváltott potenciált a primer szenzoros kéregterület felett lehet regisztrálni (36. ábra) Ez a szomatotopikus jel alkalmas az agykéreg szenzoros feltérképezésére. Kiváltott potenciál a primer területek környezetéből, illetve ettől távolabb is elvezethető (másodlagos kiváltott potenciál), melyet azonban nem a primer potenciál intrakortikális terjedése, hanem thalamikus aspecifikus projekciók hoznak létre. A másodlagos kiváltott potenciál lassúbb lefolyású, mint az elsődleges és így az elsődleges mintegy beleolvad annak kezdeti
fázisába (36. ábra) A kiváltott potenciálok az EEG-jelekkel azonos nagyságrendű és – kialakulási mechanizmusukat tekintve is – hasonló jelek. Mivel beleolvadnak a zajszerű EEG-jelbe, ezért csak jelátlagolási módszerekkel regisztrálhatók olyan tisztán, mint azt a 36. ábrán látjuk Az EEG Az agy nem csak specifikus afferentációval kiváltható elektromos válaszra képes, hanem folyamatos, „spontán” elektromos aktivitást is mutat, melyet a fülcimpához, mint referenciához viszonyítva a hajas fejbőrre helyezett elektródákkal, és kellően nagy erősítéssel regisztrálni lehet 42 (elektroenkefalográfia, EEG). A feszültségingadozások nagyságrendje µV-os (!), tehát nem tévesztendő össze a biológiai membránok mV-os nagyságrendű nyugalmi vagy akciós potenciáljának PRIMER KIVÁLTOTT POTENCIÁL (izolált, szomatotopikus) SZEKUNDER KIVÁLTOTT POTENCIÁL (kiterjedtebb, nem szomatotopikus) 200 µV Primer szenzoros kégi locus
Primer kezdeti rész + 100 ms 36. ábra Primer és szekunder agykérgi kiváltott potenciálok. (Ganong, Review of Medical Physiology, Fourteenth Edition, Fig. 11-4 és Bálint, Orvosi élettan, 1986, 94/1 ábra alapján.) 43 nagyságrendjével. Egy-egy elektróda több ezer kolumna aktivitását regisztrálja A hullámokat görög betűvel jelöljük. Az EEG-hullámok amplitúdója és frekvenciája az agy funkcionális állapotával változik (V. Táblázat) Minél kisebb az agyi működés éberségi szintje, annál szinkronizáltabb az agyi elektromos tevékenység, annál nagyobb az amplitúdó és kisebb a frekvencia. Nagyon nagy amplitúdójú hullámtevékenység kóros, és jelzi, hogy igen nagy agykérgi területekre terjed ki a normálisnál nagyobb mérvű szinkronizáció. Ezek a hullámok általában egyes EEGelvezésekben, tehát fokálisan mutatkoznak (epilepsziás görcsök) V. Táblázat EEG-hullám Normalizált amplitúdó Frekvencia (Hz) Állapot
intenzív figyelem vagy γ 0,5x (?) 30-50 β 1x 14 felett éber α ~2x 8-13 nyugalom, felületes alvás θ ~3x 4-7 közepesen mély alvás δ ~5x 0,5-3 mély alvás ~10x ~3, változó epilepsziás görcs REM-alvás Az EEG eredete Az EEG-ben tükröződő agyi elektromos tevékenység nem az agykérgi neuronok akciós potenciál sorozatainak összege. Eredete a thalamusból az agykéreg felső rétegeibe érkező aspecifikus projekció által kialakított dipólusokban keresendő, melyek az agykéregben a felszínre merőleges irányú, passzív extracelluláris ionáramokat keltenek. Az így létrejövő, alapvetően dentritikus poteciálokat rögzíti az EEG (37 ábra). 44 I. Dendritikus arborizáció II. III. Aspecifikus thalamikus afferentáció IV. V. Piramissejt test VI. ++++ EC-áram + + + + + + Aspecifikus thalamikus afferentáció 37. ábra A thalamicus aspecifikus afferenctáció és a piramissejtek kapcsolata az
agykéreg felszíni rétegeiben. Anatómiai viszonyok az ábra felső részén láthatók A piramissejt dendritjeit depolarizálja a thalamikus aspecifikus afferentáció így kialakítva egy kérgi dipólust a kérgi szinapszisok és az V. rétegben lévő piramis sejttestek között (szaggatott vonal) Az EEG-ben regisztrált feszültséget a kéreg felszínére merőlegesen folyó passzív extracelluláris áramok hozzák létre. (Ganong, Review of Medical Physiology, Fourteenth Edition, Fig 11-2 és Fonyó, Az orvosi élettan tankönyve, második kiadás, 38-2. ábra alapján) 45 Az „ébresztőrendszer” (Aszcendáló Retikularis Aktiváló Szisztéma) és az EEG deszinkronizációja A nyúltagytól az agytörzsön és a hídon át a hypothalamus környékéig hatalmas, poliszinaptikus neuronális kapcsolatban lévő idegsejt populáció, a formatio reticularis helyezkedik el. Ezekhez a neuronokhoz minden aszcendáló szenzoros pálya kollaterálisokat ad (35. ábra) A
kollaterálisokon beérkező jelek a nagyszámú poliszinaptikus kapcsolódás során felerősödnek, és a jelentős konvergencia miatt elvesztik modalitás-specificitásukat. Az aspecifikus neuronális információ (ASP 35 ábra) vagy a thalamus aspecifikus magvain átcsatolódva, vagy a thalamust megkerülve jut az agykéregbe. Ez a kérgi projekció diffúz, kiterjed minden kérgi területre. Szerepe az agy ébresztésében és a szenzoros információ feldolgozását elősegítő intenzív koncentráció fenntartásában van. Az ARAS működése nélkül az agykéreg szenzoros funkcióit nem tudja megvalósítani, ténylegesen alvó állapotba kerül. Az ARAS aktivitása az EEG-t deszikronizálja, tehát az EEG-jelek amplitúdóját csökkenti, és frekvenciáját növeli (VI. Táblázat) VI. Táblázat RELÉ (ÁTKAPCSOLÓ) Üzemmód (deszinkronizáló) DESZINKRONIZÁLT EEG-regisztrátum Tudati állapot ARAS Thalamocorticalis sejtek nyugalmi potenciálja ÉBER BE DEPOLARIZÁLT
OSZCILLÁTOR (szinkronizáló) SZINKRONIZÁLT Üzemmód EEG-regisztrátum Tudati állapot ARAS Thalamocorticalis sejtek nyugalmi potenciálja ALVÓ KI HYPERPOLARIZÁLT 46 Az EEG szinkronizációja Az a tény, hogy a több milliméternyi EEG-elektróda által „látott” több ezer piramissejt szummált dendritikus potenciáljai 0 µV-tól – azaz az izoelektromos szinttől – eltérő, formált EEG-hullámokat eredményez, azt jelenti, hogy számos agykérgi kolumna aktivitása egymással szinkron, potenciáljaik azonos fázisba kerülnek. A szinkronizáló nem specifikus afferentációt nagyrészt a thalamus tartja fenn (VI. Táblázat) A mechanizmus alapját azok a visszacsatoló körök képezik, melyeken keresztül egy, a thalamus nem specifikus magvaiból a kérgi piramissejtek dendritjeihez futó aspecifikus afferentáció egyben gátolja a projiciáló, illetve a szomszédos sejtek aktivitását. Ezek a sejtek a mintegy 100 msec-ig tartó gátlás után felszabadulva
aktív állapotba mennek át. A thalamicus oszcillátor frekvenciája függ a beérkező szenzoros ingerületektől, valamint az ébresztés szintjétől, és érzékeny a narkózisra is. 50 Hz specifikus szenzoros ingerlési frekvencia felett megszűnik az agykérgi dendritikus IPSP–EPSP-ciklus, és így az agykérgi lassú hullámú tevékenység deszinkronizálódik (átmenet az α-ritmusból a β-ritmusba). A thalamus és az agykéreg kapcsolatát jellemzi, hogy • A thalamus és az agykéreg reciprok neuronális kapcsolatban vannak. • A thalamus ritmikus aktivitása EPSP–IPSP-ciklusokat gerjeszt az agykéregben, mely szinkronizált kérgi EEG-hullámokká (α) integrálódik. • A thalamus ritmikus aktivitása az éberségi szint függvénye. • A thalamus egy kapu: ha átengedi a specifikus aszcendáló szenzoros információt, akkor egyben lehetővé teszi, hogy a kéreg azt befogadja (VI. Táblázat, RELÉ-üzemmód); ha nem, akkor a szinkronizált szerveződés
állapotában biztosítja, hogy a kéreg feldolgozhassa a korábban befogadott információt (VI. Táblázat, OSZCILLÁLÓ-üzemmód) Ébrenlét, alvás, cirkadián ritmus Az agykéreg működése nélkül nincs éber, tudatos tevékenység kivitelezésére alkalmas állapot. De láttuk, hogy az ARAS, valamint a thalamus milyen fontos szerepet játszik az agykérgi aktivitásnak az aktuális szenzoros affrerentációs szinthez történő 47 hangolásában. Megnövekedett, változatos szenzoros afferentáció, illetve ARASaktivitás az EEG deszinkronizációjához vezet, mely az éber állapot elektrofiziológia jele is egyben. A szenzoros afferentáció alacsonyabb szintje csökkenti az ARAS által kibocsátott aspecifikus neuronális efferens aktivitást, illetve csökkenő frekvencia mellett növeli a thalamus szinkronizációját. Mindez hasonló természetű változásokat idéz elő az EEG-ben is. Az éber állapottól a mély alvásig fokozatosan nő az EEGjelek
szinkronizációja (amplitúdó nő, frekvencia csökken) és csökken az éberségi szint (39. és 40 ábra) Az alvási orsók megjelenése egybeesik a tudatos percepció megszűnésével. Az alvás alatt a szinkronizáció mértéke oszcillál (V Táblázat, 41 ábra). A szinkronizáció mértéke, és így az alvás mélysége elalvás után kb 45 perc múlva a legmélyebb, majd 4-5 egyre kisebb mélységű cikluson keresztül a reggeli felébredésig ismétlődik. Idegrendszeri és testi működésünk az alvás során két, egymástól jelentősen eltérő állapotot mutat. Az egyik gyors szemmozgással (Rapid Eye Movement) párosul, ezért REM-alvásként, a másikat NREM-alvásként (Nem REM) említjük. Az NREM-alvási stádiumokban az alvás mélysége ciklusosan változik. Az izomtónus sosem szűnik meg, így az alvó időről időre változtatja testhelyzetét. Az NREM-alvás felületes stádiumában (és csakis ekkor!) az NREMalvás átvált a REM-alvásba (41 ábra) Ebben
a fázisban az alvó nehezen ébreszthető, bár spontán ébredés a felületes NREM-alvási stádiumban gyakori. A legjellemzőbb a gyors szemmozgás, az EEG deszinkronizálódik, az izomtónus (kivéve a szem-, középfül- és légzőizmokat) megszűnik. Jelentős vegetatív változások tapasztalhatók: a vér adrenalinszintje, a szívfrekvencia és a vérnyomás emelkedik, a nemiszervek véráramlása fokozódik (erekció). Ebben a fázisban intenzív az álomtevékenység, de az izomtónus hiánya miatt az álomképek motoros aspektusai nem kerülnek kivitelezésre. A REM-alvásból felébresztettek „szenzoros” jellegű álmokról számolnak be, míg az NREM-alvásra inkább a „gondolati” jellegű álmok jellemzőek. A naponta alvással töltött idő és a REM/NREM arány az élet során változik (42. ábra). Az elalvást nem az ARAS inaktiválódása idézi elő. Az alvás aktív folyamat Lassú hullámú alvás központ • a medulla középvonalában a raphe
magvakat is magában foglalva • szerotonin mediáció • léziója álmatlanságot okoz 48 ÁLLAPOT STILIZÁLT EEG-HULLÁMOK EEG-HULLÁM Éber β Nyugalom, felületes alvás α Alvási orsó Közepesen mély alvás θ δ Mély alvás 0 1 2 Idő (sec) 3 4 39. ábra Az EEG frekvenciájának és amplitudójának változása az ébrenlét-alvás ciklus kapcsán. (Bullock, Boyle III, Wang, NMS Physiology, Third Edition, Fig. 8-1 alapján) Éber Nyugalom Álmos Alvás – 2. stádium Alvás – 4. stádium 50 µV 1 sec 40. ábra Alváslaboratóriumban készült eredeti EEG-regisztrátumok 49 Átmeneti Átmene éber tiperiódusok éber Végleges ébredés REM-alvás Éber Felületes . Közepesen mély . Mély 0 1 2 3 4 5 6 IDŐ (óra) 41. ábra Az alvási stádiumok ciklikus váltakozása egy éjszaka folyamán. Mély alvásból és REM (Rapid Eye Movement)-alvásból egyaránt nehéz felébreszteni az alvót. Az éjszaka folyamán rövid
időszakokra az EEG ébredés jelét mutatja. Az alvásból történő végleges ébredésre az egyre felületesebbé váló alvási ciklusok vezetnek. (Bullock, Boyle III, Wang, NMS Physiology, Third Edition, Fig. 8-2 alapján) 100 % ALVÁS % 25 % REM % kora- új- csecsemő gyermek pubertás szülött felnőtt öreg ÉLETKOR 42. ábra Az alvás aránya a nap százalékában és a REM-alvás aránya az alvással töltött idő százalékában kifejezve az életkor függvényében 50 REM-központ • híd fomatio reticularis a locus ceruleust is magában foglalva • noradrenalin mediáció • léziója kiiktatja a REM-fázisokat Alvásra a szervezetünknek mindenképpen szüksége van. Az alváshiány destabilizálja a mentális és vegetatív funkciókat. Az alvás végleges meggátlása a szabályozási mechanizmusok széthullása miatt halálhoz vezet. Az alváshiányt szervezetünk bepótolja. Az alvási zavarok – mint pl a narkolepszia (hirtelen fellépő
REM-alvás), a katalepszia (mint előbb, de eszméletvesztés nincs), az alvajárás, ágybavizelés (gyermekeknél gyakori), rémálmok – gyógyítása fontos betegségmegelőző illetve terápiás tevékenység. Az ébrenlét–alvási ciklus periódusidejét endogén tényezők (a két nucleus suprachiasmaticus aktivitása) határozzák meg. Az endogén ciklus hosszabb, mint a 24 órás napi ciklus (cirkadián ritmus). A két suprachiasmaticus mag retinális kapcsolatai révén (retinohypothalamicus pálya) hangolja az endogén ébrenlét–alvási ritmust a nappalok és éjszakák váltakozásának 24 órás üteméhez, melyben a retinából származó fényingereknek döntő szerepe van. Emberben emellett még egyéb hatások is befolyásolják az ébrenléti és alvási periódusok hosszát. Napi ritmusban nem csak az ébrenlét, hanem a szervezet számos más funkciója is mutat periódikus változást (testhőmérséklet, hormonszintek stb.) 51 FELHASZNÁLT FORRÁSOK
Bálint, P.: Orvosi élettan, Medicina, 1986 Berne, R. M; Levy, M N; Koeppen, B M; Stanton, B A: Physiology, Fourth Edition, Mosby, 1998. Bullock, J.; Boyle, J III; Wang, M B: National Medical Series (NMS), Physiology, Third Edition, Williams and Wilkins, 1995. Fonyó, A.: Az orvosi élettan tankönyve, második kiadás, Medicina, 1999 Ganong, W. F: Review of Medical Physiology, Fourteenth Edition, Prentice-Hall international Inc., 1989 Guyton, A. C; Hall, J E: Textbook of Medical Physiology, Ninth Edition, W B Saunders Company, 1996. Silbernagl, S.; Despopoulos, A: SH atlasz Élettan, Springer Hungarica, 1994 52
felvételére azért van mód, mert az egyes receptorféleségek felépítésük és működésük alapján specializálódtak az adott energiaforma (mechanikai, kémiai, hő stb.) felvételére A receptorok egy része érzékszerveket képez (szem, fül), és speciális ingermodalitás felvételével komplex érzékelési funkciók megvalósításában vesz részt (fény–látás, hang–hallás). Ezeknek a receptoroknak a működését az élettan megfelelő fejezetei tárgyalják. A receptorok osztályozása A receptorok osztályozása különféle szempontok szerint történhet: • • • • • • inger forrása: exteroceptorok (bőr, szem, fül stb.), interoceptorok (kemo-, baro-, proprioceptorok) ingerlő energia fajtája (mechano-, thermo-, noci-, foto-, kemoreceptorok) kialakuló érzetféleség (tapintás, hideg–meleg, fájdalom, foto, halló, ízlelő, szagló) adaptáció (gyors és lassú) lokalizáció (felületi, mély, viszcerális, speciális) egyéb (tele-
vs. kontakt receptorok) 2 MECHANORECEPTOR KEMORECEPTOR FOTORECEPTOR 1. ábra A receptormembrán tulajdonságának megváltozása inger behatására különféle receptorok esetében. A közös elem, mely a receptorban elindítja az ingerületi folyamatot, a membrán ionpermeabilitásának növekedése, vagy csökkenése. (Berne and Levy, Physiology, Fourth Edition, Fig. 7-2 alapján) 3 A receptorokban az inger behatása jelet hoz létre Az érzékelés lényegi mozzanata az energiaátvitel (transzdukció), melynek során az inger behatására a receptorsejt mebrántulajdonsága megváltozik. A transzdukció eltérő modalitások esetében is az érzékelési folyamatban a közös, indító elem (1. ábra). Alapfogalmak: • • • • adekvát inger az ingerlő energiaátvitel (transzdukció) adaptáció kódolás A receptor számára adekvát inger az energiának az a fajtája, melyből már egy minimálisan elégséges mennyiség is kiváltja a receptorra jellemző
ingerület-leadást, és előidézi a receptor által kódolt modalitására jellemző érzetet. Egy receptor specificitása egyrészt a receptor sajátos szerkezetéből, másrészt pedig sajátos működéséből adódik. Ezek együttesen határozzák meg, hogy egy adott receptor számára mi az adekvát inger, tehát mi is az, amit a receptor érzékel. Az energia-transzdukció két lépésben történik. Első lépésben az ingerlő energia kapcsolatba lép a receptorsejt membránjával, és annak ionpermeabilitását megváltoztatja (1 és 2. ábra) Ennek következtében a receptor ún transducer régióján egy elsődleges helyi válasz, a receptorpotenciál (RP) alakul ki (3. ábra) Ha a receptorpotenciál meghaladja a receptor membránjára jellemző küszöbpotenciál értékét, akkor a receptor sejtmembránjának egy proximálisabb részén (generátor régió) kialakul az akciós potenciál (AP) (3. ábra) Minél nagyobb az ingerintenzitás (I), annál nagyobb a RP
amplitúdója és így az APsorozat frekvenciája is (4. ábra) I és RP közötti összefüggést a Steven-féle hatványtörvény írja le: 4 2. ábra Egy mechanoreceptor ingerlése a receptor centrumában található idegvégződés membránját deformálja, ami a membránpermeabilitást megnövelve a legközelebbi Ranvierféle befűződés irányában lokális ionáramot generál. Tovaterjedő akciós potenciál (AP) 3. ábra A receptorpotenciál az inger hatására + + + + + + + + + + + + + + + + a receptor + + + transzducer + + régióján jelenik + + + + + + + + + + + + + + meg és terjed át a proximálisan Transzducer régió AP-generáló régió elhelyezkedő akciós potenciál generáló régióra. E két régió egymáshoz való kapcsolódásának jellege adja részbeni magyarázatát az adott receptorra jellemző adaptációnak. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-3 alapján) Akciós potenciálok mV Receptorpotenciál -60
-90 Nyugalmi membránpotenciál Küszöbpotenciál 0 100 IDŐ (msec) 4. ábra Ingerlés hatására az idegvégződés membránja depolarizálódik. A depolarizáció – a receptorpotenciál – mértéke arányos az inger intenzitásával. Ha a receptorpotenciál meghaladja az adott receptorra jellemző küszöbértéket, akkor akciós potenciál keletkezik, melynek frekvenciája arányos a receptorpotenciállal, és így az ingerintenzitással. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-2 alapján) 5 VRP = k ( I − I 0 ) n ahol VRP = a receptorpotenciál nagysága k = konstans I = ingerintenzitás Io = küszöbintenzitás n = hatványkitevő, egy adott modalitásra jellemző konstans Ez az összefüggés még ismeretes egy kevésbé pontos, jóval korábban leírt alakban is (Fechner-törvény). VRP = k log I Io A hatványkitevő, n, értéke egy-egy modalitásra és receptorféleségre jellemző állandó, mely lehet n<1, n~1
vagy n>1, és ami meghatározza, hogy az adott receptor mely intenzitástartományban mutat kis – illetve melyben nagy érzékenységet (5. ábra) Látható, hogy egy bőr mechanoreceptor (n<1) igen érzékeny a kis energiatartományokban, és így igen alkalmas finom mechanikai ingerek detektálására (pl. bőr simítása) A hideg receptorok (n~1) válaszában megmutatkozó érzékenység nem függ az ingerintezitástól, míg a nociceptorok (n>1) a károsító behatás intenzitásának fokozódásával növekszik, mely egyezik azon tapasztalatunkkal, hogy ilyenkor a fájdalom jelentősen fokozódik. A receptorok egyrészt anatómiai felépítésük, másrészt a receptorfolyamatok eltérő természete miatt különböző mértékű adaptációt mutatnak. Ha folyamatos ingerbehatás mellett az AP-frekvencia az időben gyorsan csökken, a receptor gyors adaptációt mutat (fázisos vagy dinamikus receptor), ha az AP-frekvencia időbeni csökkenése 6
MECHANORECEPTOR Érzet intenzitása kis érzékenység fAP VRP nagy érzékenység I-Io HIDEGRECEPTOR Érzet intenzitása fAP VRP azonos érzékenység I-Io NOCICEPTOR nagy érzékenység Érzet Érzet intenzitása intenzitása ffAP AP log VRP VRP kis érzékenység I-Io 5. ábra Különféle receptorokat érő adekvát ingerintenzitás, I-Io, a receptorpotenciál, a receptor primer afferensének akciós potenciál frekvenciája, fAP, és a szenzoros központban kialakuló érzet erőssége közötti összefüggés (lásd Steven-féle hatványfüggvény). A receptor érzékenysége az egyes intenzitás tartományokban a hatványkitevő, n, értékétől függ. 7 nem jelentős, akkor lassú az adaptáció (tónusos vagy statikus receptorok) (6. ábra) Lassan és gyorsan adaptálódó mechanoreceptorok együttesen teszik lehetővé, hogy a bőrt érő mechanikai behatást a maga komplexitásában érzékelhessük (7. ábra) Az ingerrel kiváltott érzet időtartama
a receptor és a receptor által kialakított jel feldolgozását végző központ(ok) adaptációjától függ. Az inger (jel) kódolása Az ingerben rejlő információ kódolása történhet: • • • intenzitás szerint (frekvenciakódolás) lokalizáció szerint (kollaterális gátlás) ingerfajta szerint (jelölt pályák, modalitások és szubmodalitások) Intenzitás szerinti kódolás: Az intenzitás szerinti kódolás alapját a Steven-féle összefüggés képezi. Az eredeti információt a RP közvetítésével kiváltott AP-sorozat frekvenciája hordozza, mely a primer afferens roston terjed a központi idegrendszer irányába. A receptorban történő elsődleges kódolás technikai értelemben egy ún analóg/digitális jelátalakítás (A/D konverzió), melynek során egy adott tartományban bármely értéket felvevő receptor-potenciálból (analóg jel) kialakul egy adott frekvenciájú AP-sorozat (digitális jel). Az AP-sorozat digitális jel, mert a
frekvencia egy maximális értékkel behatárolt tartományában nem vehet fel akármilyen tetszőleges értéket, hanem csak meghatározott (diszkrét) értékeket. A kódolásra alkalmas digitális frekvenciaskála felbontását az adott receptorra és afferentációjára jellemző akciós potenciálok paraméterei, a vezetési sebesség és az ingerület szinaptikus átkapcsolásának folyamatai együttesen határozzák meg. A RP elektrotónusos tulajdonságai miatt csak helyi válasz kialakítására alkalmas, hosszabb távon amplitúdója folyamatosan és jelentősen csökken, ezért információ továbbítására nem alkalmas. Az AP viszont terjedése közben hosszabb távon sem veszít amplitúdójából, mivel terjedését az idegrost aktív membránfolyamatai (Hodgkinciklus) biztosítják. Az információ kódolásában az A/D jelátalakításnak tehát előnye az, hogy egy lokális, analóg jelből (RP), az információtartalom megőrzését biztosító, jelentős
távolságú továbbításra alkalmas új kód (frekvenciakód) születik. Ez a kód 8 INGER 6. ábra Lassan adaptálódó receptor primer afferensén az akciós potenciálok frekvenciája folyamatos ingerlés esetén időben csak kis mértékben csökken, míg a gyorsan adaptálódó receptor esetében egy-két akciós potenciál kialakulása után megszűnik a receptorválasz. Lassan adaptálódó (statikus), pl. ín-, izomorsó 100 % Gyorsan adaptálódó (dinamikus), pl. Pacini-test fAP 0% IDŐ POZÍCIÓ Adaptáció SEBESSÉG GYORSULÁS INGER 7. ábra Statikus és dinamikus mechanoreceptorok együttesen teszik lehetővé, hogy a bőrt érő mechanikai ingert a maga komplexitásában érzékelhessük. (Berne and Levy, Physiology, Fourth Edition, Fig. 7-4 alapján.) IDŐ Jelkonverzió D/A Receptor A/D D/A A/D D/A A/D A/D A Kód A D A D A D A D 8. ábra Analóg (A) és digitális (D) kód váltakozása a szenzoros információ neuronról neuronra
történő terjedésekor. A jel terjedése digitális, feldolgozása analóg formában történik 9 nem érzékeny sem az elektromos zajra, sem pedig az egymás mellett futó idegrostokon történő „adatforgalomra”. A kódolás lényeges eleme, hogy az A/D jelátalakítás a receptortól a felsőbb idegrendszeri központokig a szinaptikus átkapcsolódással kapcsolatban többször ismétlődik (8. ábra) Egy-egy szinapszishoz érkezvén ugyanis az AP-sorozat hatására a preszinaptikus membránon mediátor molekulák jutnak a szinaptikus résbe (mennyiségük az AP-sorozat frekvenciájának függvénye), majd diffundálnak a posztszinaptikus membránhoz, ahol egy újabb helyi, analóg választ váltanak ki (posztszinaptikus potenciál, D/A konverzió). Ez utóbbi az AP kialakítására képes membránrészre terjedve AP-sorozatot vált ki (A/D konverzió), melynek frekvenciája megegyezik a preszinaptikus AP-sorozat frekvenciájával. Ilyen módon az adekvát ingerre
vonatkozó, a receptorban kódolt információ ismételt A/D és D/A konverziók révén jut az afferens pályán a felsőbb központokhoz. A lokalizáció szerinti kódolás: Minden receptor, annak primer afferense, valamint további posztszinaptikus kapcsolatai receptív mezővel jellemezhetők (9. ábra) A receptív mező a térnek az a része, amelyből származó küszöb feletti adekvát ingerek a receptorban ingerületi folyamatot váltanak ki. A receptív mező a kontakt receptorokat körülvevő tér (tapintási receptorok), míg a telereceptorok esetében ez a térnek egy a receptortól távol eső része (fotoreceptorok). A térben elosztott receptorok (pl a bőrben lévő tapintási receptorok, vagy a retinában elhelyezkedő fotoreceptorok) valamelyikét érő inger helyét azáltal tudjuk meghatározni, hogy a receptorok térbeli elhelyezkedése, és a belőlük kiinduló ingerületi folyamatnak az agykérgi feldolgozóközpontokba történő vetülése (projekciója)
bizonyos szabályszerűséget követve megfelel egymásnak. Az ingerületi folyamat terjedésének, és a jelátkapcsolás valamint -feldolgozás térbeli organizációjának az ingerelt receptorok tényleges térbeli helyzetéhez való viszonyát a topológia jellemzi. A topológia akkor megtartott, ha az átkapcsolódási pontokon (szinapszisok) a párhuzamosan futó preszinaptikus rostok nem kapcsolódnak azonos posztszinaptikus neuronra. Az egymás mellett futó pre- és posztszinaptikus axonok ugyanakkor serkentő és gátló kollaterálisaikon keresztül egymással előre- illetve visszacsatolt kapcsolatot létesítenek (pl. kollaterális vagy széli gátlás), melynek alapján lehetséges az egymáshoz térben igen közeli ingerek elkülönítése (térbeli diszkrimináció). A kollaterális gátlás úgy növeli meg a térbeli diszkriminációt (csökkenti le a posztszinaptikus receptív mezők méretét), hogy két 10 + + 9. ábra Divergencia, konvergencia. A receptív
mező akkor megtartott, ha a szenzoros információ legfeljebb csak elágazódik (divergencia), de a posztszinaptikus neuronra más neuron nem szinaptizál (konvergencia). Egy posztszinaptikus neuron egyesíti a rá konvergáló preszinaptikus neuronok receptív mezőjét (középen). 10. ábra Kollaterális gátlás. Két egymáshoz térben közeleső inger egyidejű alkalmazásakor az egymást átfedő receptív mezők miatt a primer vagy szekunder afferensek frekvenciája alapján a két inger biztosan nem különíthető el egymástól. A meglévő kismérvű különbség a gátló jellegű kollaterális kapcsolatok miatt azonban posztszinaptikusan megnő. Ez a mechanizmus kiemeli a jel kontrasztját és így megkönnyti az ingerületi mintázat valósághű feldolgozását. 11 egymáshoz térben közeli inger esetén, az ingermaximumok közé eső receptív mezőből gátolja a posztszinaptikus afferentációt (10. ábra) Az inger fajtája szerinti kódolás: Az
ingerfajtára jellemző érzet kialakulását a receptor–pálya–központ együttesen határozza meg. A kódolás módja történhet az alábbiak szerint. • Jelölt pályák (alapvető modalitások, és szubmodalitások) • Mintázatok (ízérzés – térbeli, hőérzés – időbeli) • Tulajdonság detektorok (látás) Modalitáson az inger által keltett érzet minőségét, jellegét értjük. Az alapvető modalitások kódolása ún. jelölt pályákkal történik (pályán itt a receptor–pálya– központ együttest kell értenünk). A jelölt pálya bármely elemének (elektromos) ingerlése mindig azonos, a pálya által kódolt érzet kialakulására vezet. Ebből adódik, hogy a jelölt pálya érzet kialakulását akkor is lehetővé teszi, ha az nem párosul tényleges inger jelenlétével (hallucináció). Ezt a kódolási formát általában jól meghatározható topológia jellemzi. Jóval összetettebb érzet kialakulását teszi lehetővé az időbeli
és térbeli mintázatok alapján való kódolás. Az időbeli mintázatokkal történő kódolás esetében egy neuron többféle információt is továbbíthat aszerint, hogy a jelek időbeli mintázata milyen. A hidegreceptorok afferensein például 30 oC alatt csak spontán kisülés, míg 30 oC felett a hőmérséklet emelkedésével változó jellegű csoportos kisülések (burst) jelennek meg – ezzel, és nem az átlagos kisülési frekvenciával kódolva a hőmérséklet változását. A térbeli mintázatokkal történő kódolásra példa az ízérzés. A keserű és sós íz érzetét egy hármas neuronpopuláció ingerülete hozza létre. Keserű ízt akkor érzünk, ha mindhárom, sósat, pedig ha a háromból csak kettő kerül ingerületbe. A szenzoros kódolás kifinomultabb mechanizmusait a tulajdonság-detektorokban integrált neuronok működése hozza létre. Ezek az agykéregben található neuroncsoportok, melyek akkor kerülnek ingerületi állapotba, ha
összetett szenzoros bemeneti kapcsolataikon egy bizonyos komplex ingeregyüttes jelenik meg (pl. taktilis, optikai vagy akusztikus mintázatok észlelése). 12 A BŐR SZENZOROS FUNKCIÓJA A bőr testünk felületét teljes mértékben beborítja, így a külső környezetből származó ingerek első sorban a bőrt érik. A bőrt megközelítőleg egymillió idegrost innerválja Legnagyobb részük a durva mechanikus érzékelésben játszik szerepet. Egy kicsiny, de annál fontosabb részük kódolja az alábbi finom taktilis és egyéb modalitásokat: • finom mechanikus ingerek (tapintás, vibráció, nyomás) • hőingerek (hideg, meleg) • károsító, nociceptív ingerek (fájdalom) A mechanikus ingerek érzékelését gyorsan, és lassan adaptálódó mechanoreceptorok végzik. Felépítésük, működésük valamint a bőrben történő elhelyezkedésük alapján képesek a mechanikai ingerek sokaságából az alábbi szubmodalitások kiválasztására
és kódolására. I. Táblázat Receptor Receptív mező Adaptáció Kódolt szubmodalitás Pacini-testek nagy nagyon gyors vibráció Meissner-féle testecskék kicsi gyors sebesség Merkel-féle tapintókorongok kicsi lassú lokalizáció Ruffini-testek nagy lassú időtartam és intenzitás (Gyorsan adaptálódó mechanoreceptor a szőrtüszőreceptor is.) A 6. ábrán láttuk, hogy a Pacini-test folyamatos mechanikus ingerlés ellenére igen gyorsan beszünteti ingerület-leadását, tehát adaptációja nagyon gyors. Ennek egyik oka az, hogy a receptor centrumában található csupasz, ingerlékeny idegvégződést hagymalevélszerűen egy viszonylag nagyméretű burok borítja (11/A ábra). Ha a receptort nem túl hirtelen alkalmazott, folyamatos jellegű mechanikai inger éri, akkor az energia nagy része a lemezek egymáson történő elmozdítására fordítódik, így elegendő intenzitású mechanikai energia az idegvégződést nem éri, ezért azon
sem receptorpotenciál, sem akciós potenciál sorozat nem alakulhat ki (11/B ábra). Ha viszont a receptorral a mechanikai 13 ingert kellő intenzitásban és A Lamellált burok Idegvégződés Ingerlési mintázat B A lamellák átrendeződésére van kellő idő, így inger nem éri az idegvégződést Nincs afferens ingerület C A lemellák átrendeződésére idő nincs, így a jelentős lokális lamelláris deformáció az inger energiáját közvetíti a receptor membránjához Van afferens ingerület 11. ábra Egy gyorsan adaptálódó (dinamikus, fázikus) mechanoreceptor (A) válasza nem túlságosan hirtelen elkezdett és folyamatosan fenntartott (B) valamint rövid idejű és gyakran ismétlődő (C) mechanikai ingerlésre (vibráció) 14 kellően gyorsan közöljük, a lemezek a hirtelen energiabehatásra lokálisan deformálódnak, így mintegy utat engednek az energia terjedésének egészen az idegvégződésig, ahol a membrán deformációja
receptorpotenciál és következményes akciós potenciál sorozat kialakulását eredményezi (11/C és 12. ábra) Mindeközben a lemezek globális pozíciója nem változik jelentősen, mivel az átrendeződésre a gyors dinamika miatt nincs lehetőség. A Pacini-test receptív mezője nagy, mert a vibrációs energia terjedése a bőr szövetében nem okoz jelentős átrendeződést, és így a receptort távolabbról is érik vibrációs hatások. A Meissner-féle testecskék tokja jóval kisebb, és ezért csak közvetlenül a receptor feletti bőrrészlet ingerlése vezet AP-leadásra. A receptor csak akkor válaszol, ha az inger időben folyamatosan változik (12. ábra), ami például ujjainknak egy érdes felületen történő futtatásakor fordul elő. Érzékelésre valójában a mechanikai inger sebessége kerül (7. ábra) A Merkel-féle tapintókorongok speciálisak abban a tekintetben, hogy a tulajdonképpeni receptor nem az idegvégződés, hanem azok az
epiteliális sejtek, melyek a tapintókorongot alkotják. Ezek a sejtek szinaptizálnak a receptort innerváló idegrosttal. A receptor lassú adaptációja, felületes elhelyezkedése (13 ábra) és kis receptív mezője alkalmassá teszi a mechanikus inger (a bőr megnyomása) lokalizációjának kódolására. A Ruffini-testek folyadékkal teli kollagén tokkal körülvett idegvégződésből állnak: a tokot az idegvégződéshez (befelé) és a bőrhöz (kifelé) kollagén kötegek rögzítik. A nagy receptív mező és lassú adaptáció alkalmassá teszi a bőrt érő folyamatos mechanikai behatás (a bőr deformációja, elmozdulása, gyűrődése) mértékének kódolására mindaddig, míg az ingerhatás tart. A mechanoreceptorok bőrben való elhelyezkedése a természet logikáját követi, mely szerint a finom taktilis információt közvetítő Meissner-féle testecskék, Merkel-féle tapintókorongok és a szőrtüszőreceptorok a bőrben a lehető legfelületesebben
helyezkednek el, míg a vibrációt kódoló Pacini-testek a mélyebb rétegekben találhatók (13. ábra) 15 INGERLÉSI FORMA AFFERENS AP-SOROZAT log fAP log A bőrre ható nyomás intenzitása log A bőrre ható nyomás által előidézett deformáció sebessége log A mechanikai deformáció gyorsulása, mely azonos a vibráció frekvenciájával 12. ábra A bőrt érő mechanikus ingerek érzékelésének formái. A különféle mechanoreceptorok a mechanikai inger egy-egy jellemző tulajdonságára érzékenyek. Ezért az inger által keltett jelek feldolgozása már receptorszinten elkezdődik. A feldolgozás az agykérgi szinten fejeződik be és alakul ki a mechanikai inger által keltett érzet a maga komplexitásában. (SilbernaglDespopoulos, SH atlasz Élettan, 1994, 288. oldal B ábra alapján) SZŐRÖS BŐR SZŐRTELEN BŐR SZARURÉTEG Tapintás Tapintás Érintés FELHÁM Érintés IRHA KÖTŐSZÖVET Vibráció Merkel-sejt és -korong Meissner-féle
testecske Pacini-test Szőrtüsző receptor 13. ábra A bőr mechanoreceptorainak eloszlása. A bőrben az érintésre és nyomásra érzékeny receptorok felületesen, a vibrációra érzékenyek mélyebben helyezkednek el. (SilbernaglDespopoulos, SH atlasz Élettan, 1994, 288 oldal A ábra alapján) 16 Lassan és gyorsan adaptálódó mechanoreceptorok együttesen teszik lehetőve, hogy a bőrt érő mechanikai behatást a maga komplexitásában érzékelhessük (7. ábra) A hő érzékelését a bőrben két receptorféleség, a hideg- és melegreceptorok végzik. Ezek Aδ és C csoportba tartozó szabad idegvégződések, melyek AP-leadása statikus ingerlés esetén eltérő eloszlást mutat (14. ábra) Neutrális hőmérsékleti tartományban ezek a receptorok egyaránt spontán kisülést és teljes adaptációt mutatnak. Ezért kellemes hőmérsékleti körülmények között nem alakul ki bennünk egy folyamatos hőérzet. Ezeknek a receptoroknak a dinamikus válasza
egymás tükörképei: a hőmérséklet csökkenésére a hideg receptorok válasza átmenetileg nő, a melegeké átmenetileg csökken, a hőmérséklet emelkedésére pedig fordítva (15. ábra) A neutrális tartomány alatti hőmérsékletek kódolása a hidegreceptorok burst-szerű aktivitása alapján történik, mely a temporális mintázat alapján történő érzékelés egyik példája (16. ábra) Vegyük észre (14 ábra), hogy ebben a tartományban a hideg receptorok statikus hőingerre azonos kisülési frekvenciával válaszolnak, tehát a hőmérsékletet statikus aktivitásukkal nem kódolhatják! Hőérzetünket befolyásolja a megérintett tárgyak anyagi minősége is. Azonos hőmérsékletű fém- és fa tárgy közül a fémtárgyat hidegebbnek érezzük, mert a fémtárgy a bőrből több hőt von el, és így a hőreceptorok átlagosan alacsonyabb hőmérsékletre kerülnek valamint a megérintést követő hőtranziens is nagyobb (15. és 17 ábra) A bőr
hőmérséklete befolyásolja a hőérzetet azért is, mert – mint láttuk (15. ábra) – a hőreceptorok válasza a hőbehatásra tranziens jellegű, így a 35 oC-os hőmérsékletet hidegnek érezzük, ha bőrünk 40 oC-os, míg melegnek, ha az 30 oC-os. Hőérzetünk stabil hőhatás alatt a 18 ábrán feltüntetett módon a még károsodáshoz nem vezető hideg hőmérsékletektől (>0 o C) a már károsodáshoz vezető hőmérsékletekig (>45 oC) a hideg–neutrális–meleg– forró majd fájdalmas átmenetek szerint alakul. A 45–49 oC közötti tartományban a hideg- és fájdalomreceptorok leadása fokozódik, ezért a forró érzet kialakulása előtt paradox hideg- és fájdalomérzés jelentkezik. A szöveti károsodással járó ún. nociceptív ingereket szintén Aδ- és C-csoportba tartozó szabad idegvégződések veszik fel. Ezek ingerülete fájdalommal jár, mely 17 Melegreceptrok Neutrális tartomány Hidegreceptorok fAP 20 Paradox
hidegérzés 30 40 50 o C ÁLLANDÓSULT BŐRHŐMÉRSÉKLET 14. ábra A bőr thermoreceptorainak válasza állandósult bőrhőmérsékletű hőingerekre T = 33 oC Spontán kisülés! T = 30 oC HIDEGRECEPTOR MELEGRECEPTOR 15. ábra A bőr thermoreceptorainak válasza tranziens hőingerekre. (Bullock, Boyle III, Wang, NMS Physiology, Third Edition, Fig. 5-5 alapján) T = 34 oC ∆T ∆T = 4 oC ∆T = 6 oC 16. ábra Hőinger kódolása temporális mintázattal (hidegreceptorok burst-aktivitása) 18 30 oC FATÁRGY melegebbnek érezzük 30 oC FÉMTÁRGY hidegebbnek érezzük 17. ábra A hőérzet függ a megérintett tárgy anyagi minőségétől is. A bőrhőmérséklet eloszlását ú.n izotermikus vonalakkal jelöltük Mint látható, a fémtárgy nagyobb hőelvonása miatt a fémtárggyal érintkező bőr jobban lehűl, mint a fatárgy alatt. o C FÁJDALOM KÁROSODÁS 45 35 MELEG NEUTRÁLIS ADAPTÁCIÓ 32 HIDEG 18. ábra Az állandósult hőérzet és a
receptor funkcionális állapotai közötti kapcsolat 19 vitális jelentőségű, hiszen tudatosodás esetén felhívja az élőlény figyelmét a folyamatban lévő, szöveteit károsító folyamatra. A bőr nociceptorainak adekvát ingere pontosan nem ismert, de feltételezhető, hogy a fájdalmas stimulust a sejtek károsodásakor felszabadult kémiai anyagok, mint pl. hisztamin és bradykinin jelentik. A korábbi elképzelés – miszerint a kiváltott fájdalom a bőrben lévő mechano- vagy kemoreceptorok túlingerlésének volna köszönhető –, mára már tarthatatlanná vált. A károsító ágensek specifikus nociceptorok ingerületével váltják ki a fájdalmat. Ezeknek jellemzője, hogy szabad idegvégződések, és nincs jelátalakító burkuk (19. ábra) II. Táblázat Nociceptor Innerváló rost Specifikus Polimodális Aδ C kémiai termikus mechanikus Inger forró + K , serotonin, bradykinin, hisztamin hideg Mediáció glutamát glutamát
és P-anyag Vezetés gyors (12-30 m/s) lassú (0,5-2 m/s) lokalizált diffúz Lokalizáció Mint azt az 5. ábrán láthattuk, a nociceptorok ingerülete a károsító inger intenzitásával exponenciálisan nő, melynek oka ezen receptorok szenzitizációjában, az ingerbehatásra bekövetkező érzékenyülésében keresendő. Ennek egyik mechanizmusa a 19. ábrán látható A primer károsító inger sejtkárosodással jár, melynek folyamán az elhaló sejtből proteolítikus enzimek szabadulnak fel, melyek a keringő γ-globulinokból bradykinint hasítanak le. A bradykinin-molekulák a szabad nonciceptív idegvégződés membránjához kötődve másodlagos hírvivő mechanizmuson keresztül az idegvégződést érzékenyebbé teszik. A sejtkárosodási folyamat előrehaladtával ez a folyamat önerősítő jelleggel folytatódik (circulus vitiosus), mely magyarázza a nociceptív ingerület-leadás exponenciális fokozódását és azt, hogy kismértékű
ingerintenzitás növekedés a fájdalom jelentős fokozódásával jár. 20 A szenzitizációnak egyéb mechanizmusai is vannak, melyek mediátorai különféle anyagok lehetnek (K+, szerotonin, prosztaglandinok). Régóta megfigyelt jelenség, hogy a bőrt érő különféle károsító behatás bőrpírral, a bőr duzzanatával, a bőr hőmérséklet lokális emelkedésével, valamint fájdalmasságával jár. Ezeket a tüneteket a klinikumban rubor, tumor, calor és dolor latin szavakkal jelöli. Kialakulásuk mechanizmusát sematikusan a 20. ábra szemlélteti A károsító inger által keltett primer ingerületi folyamat az ingerlés helyétől antidrómos irányban terjed a szomszédos szabad idegvégződésekhez (axon reflex), ahol P-anyag és calcitonin gene-related peptide (CGRP) felszabadulását idézi elő. Ezek az anyagok a helyi környezet megváltozását okozzák, egyrészt azzal, hogy az erek falához diffundálva dilatálják azokat. Ennek eredménye a bőrpír
(rubor) és a fokozott véráramlás miatti bőrhőmérséklet-emelkedés (calor). Ezek az anyagok megnövelik az érfal (kapilláris, venula) permeabilitását, és így fokozzák a filtráció irányú Starling-erőket azáltal, hogy előidézik a plazmafehérjék extravazációját, ami fokozza az interstícium kolloid ozmotikus nyomását. Ennek eredménye a interstíciumban a szabadvíz felszaporodása, az ödéma (tumor). 21 Bőr Noxa bradykinin Nociceptív idegrost γ-globulinok Proteolítikus enzimek Nociceptív transducer Elhaló sejt 19. ábra A bőr nociceptorok szenzitizációjának egyik mechanizmusa. (Berne and Levy, Physiology, Fourth Edition, Fig. 8-5A alapján) Mikrocirkulációs érhálózat Noxa Bőr Nociceptív idegrost 2. P-anyag felszabadulás Nociceptív terminál 1. Akciós potenciál antidrómos érkezése 4. Plazma extravazáció 3. Fokozott mikrorcirkulációs áramlás és permeabilitás 20. ábra A bőrt érő nociceptív behatás által
kiváltott klinikai tünetek („color, rubor, dolor, calor”) kialakulásának mechanizmusa. (Berne and Levy, Physiology, Fourth Edition, Fig 8-5B alapján.) 22 SZOMATOSZENZOROS AFFERENTÁCIÓ A receptorok által felvett ingerek a periférián a receptorokat innerváló primer neuronon frekvencia kódban jelennek meg. A kódolt jel centrifugális irányban terjed a jelfeldolgozást végző központok felé. Egy idegrost csakis egy modalitást közvetít Az idegrostok átmérője, vezetési sebessége és az általuk innervált receptor modalitása szoros és logikus funkcionális kapcsolatban állnak (III. Táblázat ) III. Táblázat (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-6 alapján) Myelin-hüvely Myelinizált nélküli Rostátmérő (mikrométer) 20 15 10 5 1 2 0.5 6 2 0.5 Vezetési sebesség (m/s) 120 90 60 30 ÁLTALÁNOS OSZTÁLYOZÁS A C α β γ δ Izomorsó (primer) Izomorsó (szekunder) Szőrtüszőreceptor Vibráció
(Pacini-test) Finom tapintás (Meissner-féle testecskék) Durva tapintás/nyomás Mély nyomás és tapintás Akut fájdalom Krónikus fájdalom Hidegérzés Melegérzés HÁTSÓ KÖTEGLEMNISCUS MEDIALIS RENDSZER ANTEROLATERÁLIS RENDSZER 23 A gerincvelő hátsó szarva, mint a primer afferentáció átkapcsolódási helye A központi idegrendszeri projekció során a jel a szinapszisokban többször átkapcsolódik, tehát egy afferens pálya több neuronból áll (elsődleges, másodlagos, harmadlagos stb. neuronok) Az átkapcsolódásra az első lehetőség a gerincvelő hátsó szarvában van (21. ábra), melynek szerkezete lamináris (Rexed-laminák) Egy-egy laminában általában azonos típusú rostok szinaptizálnak (Aδ, C, Aβ, stb.) Minden átkapcsolódás egyben a jel által kódolt információ feldolgozására ad lehetőséget azáltal, hogy a jel digitális formából (frekvenciakód) a posztszinaptikus membránon analóg formára vált. Az analóg jelek
(EPSP-k vagy IPSP-k) a posztszinaptikus membránon az elektrotónusos feszültségek szabályszerűségei szerint integrálódnak, és így nagy gyorsasággal kialakul az az eredő, kimeneti jel, mely ismét digitális formában terjed tovább a következő szinapszisig. Egy neuron elágazó axonterminálisai számos kapcsolatot létesítenek a posztszinaptikus sejtekkel Ezek között vannak olyan sejtek is – az interneuronok –, melyek nem az aszcendáló kapcsolat elemét képezik (tehát nem szekunder vagy tercier neuronok), hanem kollaterális kapcsolatot teremtenek az aszcendáló pálya neuronjai és az adott átkapcsolódási környezet egyéb neuronjai között. Az interneuronok által kialakuló kapcsolat lehet serkentő vagy gátló jellegű, előre- vagy visszairányuló (rekurrens). Ezek a sejtek a szenzoros információ alacsonyrendű feldolgozásának elemei, melyek modalitásspecificitást mutatnak. A gerincvelő hátsó szarvának neurokémiája igen változatos,
mediátorai között szerepelnek a katecholaminok, aminosavak, szomatosztatin, Panyag, endogén opiátok stb. Aδ 21. ábra A gerincvelő hátsó szarvának lamináris szerkezete (Rexedlaminák). Ezekben a rétegekben találhatók egyes receptorok (hő, fájdalom, durva tapintás) másodlagos afferensei illetve nagyszámú interneuron, melyek a gerincvelői szenzoros jelfeldolgozás fontos elemei. C Aβ 24 Feldolgozási lehetőségek az afferens jel központi idegrendszeri átkapcsolódásai során Egy-egy roston belül az adott modalitású jel különböző intenzitásainak továbbítására kétféle lehetőség van. Ha az egyre erősebb inger egyre több receptív mezőt hoz ingerületbe, és így a roston belül egyre több neuron, illetve annak axonja kerül ingerületbe (22. ábra), térbeli szummációról beszélünk A másik lehetőség az időbeli szummáción alapul, amikor is az inger intenzitásával arányosan változik egy adott axon kisülési frekvenciája. A
szinaptikus áttevődés a jelfeldolgozás egyik alapvető lehetősége, mert a szinaptikus válasz kialakítása az analóg posztszinaptikus potenciálok integrálása révén történik. A feldolgozás komplexitását növeli, ha a jelfeldolgozásban több neuron vesz részt. Valóban, a központi idegrendszer különböző részein a neuronok anatómiai és egyben funkcionálisan szervezett csoportokat (pool) alkotnak. Ezek bemenetét igen gazdag elágazódási mintázatot mutató axonok alkotják. Egy erősen leegyszerűsített példát látunk a 23. ábrán A pool-ba belépő afferensek (B1 és B2) a valóságban ezres nagyságrendben finom terminális rostokra oszlanak, melyek gazdagon szinaptizálnak a pool neuronjainak dendritjein és somáján. A dendritek a valóságban szintén dúsan arborizáltak, így jelentősen megnövelve a bejövő szinaptikus kapcsolatok számára a kapcsolódási felületet. Az afferens kapcsolatok ily módon innervációs mezőket alkotnak. Vannak
a pool-ban olyan neuronok, melyek egy-egy afferens innervációs mezőjének középpontjában helyezkednek el, vannak olyan sejtek is, melyekkel több afferens is szinaptizál (a K3-kimenetet adó sejt) és vannak olyanok is, melyek egy adott afferenshez viszonyítva periférikus helyzetűek, rajtuk csak kis számú szinapszis található (a K1-kimenetet adó sejt). Egyetlen preszinaptikus akciós potenciál (AP) egyetlen szinaptikus kapcsolatban nem vált ki posztszinaptikus AP-t, csak EPSP-t vagy IPSP-t. A preszinaptikus rostok arborizációja biztosítja, hogy ez megtörténhessen, tehát a beérkező jel szinaptikus átkapcsolódása biztosított legyen. Az ingerlési mezők középpontjában, illetve ezek átfedéseiben lévő sejtek egy beérkező AP hatására biztosan tüzelni fognak, hiszen kellő számú szinaptikus kapcsolat egyidejű (térbeli szummáció) vagy egymást időben gyorsan követő (időbeli 25 GYENGE INGER Receptív mezők Idegrost KÖZEPESEN
ERŐS INGER ERŐS INGER 22. ábra Jelintenzitás továbbítása térbeli szummációval 26 Idegrost keresztmetsze B1 K1 K2 K3 B2 K4 23. ábra Egy neuroncsoport (pool) viszonya a gazdagon elágazó afferens végződésekhez. Számos afferens végkészülék szinaptizál egyetlen neuronnal. Szummált posztszinaptikus potenciáljaik biztosítják, hogy az afferens ingerület biztosan továbbjusson a szinapszison. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-9 alapján) BEMENET KIMENETEK POOL Kisülési zóna Facilitált zóna 24. ábra A neuroncsoporton belüli ingerlékenységi szintek. A pool centrumában lévő sejtek elegendő számú afferens jelet kapnak ahhoz, hogy biztosan küszöb feletti, kisülési állapotba kerüljenek. A kisülési zónát körülvevő területen a neuronok ingerületi állapota facilitált, mert a beérkező afferentáció nem elégséges ugyan akciós potenciál kiváltásához, de már bizonyos mértékű
depolarizációt kivált – így érzékenyebbé téve a neuront a további afferens ingerületekre. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig 46-10 alapján.) 27 szummáció) ingerületi állapota biztosítja a posztszinaptikus membránterületek küszöböt meghaladó depolarizációját (24. ábra) A kisülési (discharge) zóna környékén található neuronok is részesednek az afferens szinaptikus kapcsolatból, de nem elegendő számban, vagy időben nem kellő gyakorisággal ahhoz, hogy arra AP-lal válaszoljanak. Az őket érő afferentáció hatására ezen sejtek nyugalmi állapota megszűnik, membránpotenciáljuk közelebb kerül a küszöbpotenciálhoz, tehát facilitált állapotba kerülnek. Ebben az állapotban már egyetlen küszöb alatti erősségű afferens jel is kiválthatja kimenetükön a választ. Ha az afferentáció gátló jellegű, akkor is érvényesül a fent leírt jelenség, azonban ellenkező előjellel. A pool-t
alkotó neuronpolpulációt érő serkentő és gátló befolyások tehát a pool-on belül térben és időben az ingerületi állapot bonyolult mintázatát eredményezik. Ezek a mintázatok a pool anatómiai és funkcionális organizációjának szabályai szerint alakítják a pool kimenetén a jelmintázatot. A neuronális polpuláció tagjai között alapvetően háromféle kapcsolat van. Az egyik lehetőség, amikor egy preszinaptikus neuron egy posztszinaptikus neuronnal szinaptizál (1:1 kapcsolat). A jelfeldolgozás szempontjából ebbe a kapcsolatba kollaterális facilitáció vagy gátlás révén lehet beavatkozni, melynek eredményeként a posztszinaptikus neuronon a jel továbbítása biztosított, vagy blokkolódik (lásd a széli gátlás jelenségét). Az ingerületi folyamat központi idegrendszeri terjedésében a jelfeldolgozás másik két lehetősége a divergencia (25. ábra) és a konvergencia (26 ábra). Divergens kapcsolatok funkcionális értelemben
erősítőként működnek, illetve lehetővé teszik, hogy az afferens információn több feldolgozó központ osztozzék (pl. a hátsó kötegben aszcendáló proprioceptív afferentáció leágazása a cerebelláris magvak felé). Egyetlen afferens elágazásaiból származó konvergens kapcsolatok (lásd fenn) biztosítják, hogy a posztszinaptikus neuron biztosan válaszoljon az afferens jelre (26/A ábra). A több forrásból érkező afferentáció (26/B ábra) különféle jelfeldolgozási művelet elvégzésére – mint integrálás, összehasonlítás, rendezés – nyújt lehetőséget. A konvergencia a posztszinaptikus neuron receptív mezőjének méretét növeli, illetve modalitását megváltoztathatja (unimodális–polimodális átalakulás). 28 25. ábra Divergens neuronhálózatok. Funkcionálisan erősítési, elosztási, szenzoros vagy motoros kópia készítési szerepük van. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-11
alapján) A B 26. ábra Konvergens neuronhálózatok. Funkcionálisan biztosítják a szinaptikus kapcsolat megbízhatóságát, és összegző (integráló), összahasonlító, rendező szerepük van. (Guyton and Hall, Textbook of Medical Physiology, Ninth Edition, Fig. 46-12 alapján) 29 A felszálló szomatoszenzoros rendszerek működése A különböző modalitások elkülönülten terjednek a nagy felszálló rendszerek rostjaiban. A legjelentősebbek a hátsó köteg–lemniscus medialis rendszer (HK–LM), és az anterolaterális rendszer (AL) (27. ábra) A trigeminalis rendszer a HK–LMrendszerrel analóg elven épül fel A hátsó köteg–lemniscus medialis rendszer: • A primer afferensek 20%-át tartalmazza • Modalitások: diszkriminatív tapintás, kinesztézia, propriocepció (lásd a III. táblázatot) • Gyorsan vezető rostok (lásd a III. táblázatot) • Szigorú szomatotópia • A rostok modalitás specifikusak vagy polimodálisak •
Átkapcsolódás a hátsókötegi magvakban • Másodlagos neuron: a hátsókötegi magvakból a lemniscus medialis-szal projiciál a thalamusba • Másodlagos projekció a thalamus VPL magjába • A rendszer NEM tartalmaz nociceptív rostokat A HK-magvak (ncl. gracilis et cuneatus) átkapcsoló (relay) sejtjei glutamát, míg a preszinaptikus gátló sejtek GABA-mediációval működnek. A HK–LM-rendszerben reprezentált taktilis modalitások között nem szerepel a durva tapintás, ez ugyanis az AL-rendszerhez tartozó tr. spinthalamicuson keresztül aszcendál (28. ábra) A taktilis információ kétszeres reprezentációja miatt csak a gerincvelő kiterjedt sérülései járnak súlyos taktilis deficittel. A HK–LM-rendszer által továbbított taktilis információ finom tapintásra, nyomásra, alacsony (lebegés vagy „flutter”) és magas frekvenciájú vibrációra épülő részletes analízist tesz lehetővé, melynek nagy a gnosztikus értéke. A
propriocepció vagy sajátérzékelés lehetővé teszi, hogy tudatos vagy reflex-szintű információnk legyen ízületeink helyzetéről, izmaink tónusáról, általuk megvalósuló mozgások dinamizmusáról (kinesztézia), és testünk helyzetéről (29. ábra) Ezekhez a funkciókhoz természetesen gyorsan vezető rostok által megteremtett afferens kapcsolatok szükségesek (III. Táblázat) A rendszert szigorú szomatotópia jellemzi. Az alacsonyabb gerincvelői szinten belépő afferenseket a felsőbb szinteken belépők mediális irányba szorítják, ezért a hátsó 30 kötegben a topológiai viszonyokat tükröző ú.n szenzoros homunculus helyzete lábbal a középvonal irányába mutat, a HK-magvakkal felépülése a nyakkal zárul. Fejét majd HÁTSÓ KÖTEG LEMNISCUS MEDIALIS RENDSZER ANTEROLATERALIS RENDSZER Leminscus medialis Tr. spinothalamicus ventralis 27. ábra A gerincvelő két legfontosabb aszcendáló rendszere, a hátsó köteglemniscus medialis és
az anterolateralis rendszer. Figyeljük, meg, hogy a HK–LM-rendszer átkapcsolódás nélkül, míg az AL-rendszer hátsószarvi átkapcsolódás és zömmel az ellenoldalra történő átlépés után kezdi meg felszállását a felsőbb központok felé. Ezért a HK–LM-rendszerben a felszálló ág primer, míg az AL-rendszerben szekunder neuron. Hátsó köteg magvak Finom lokalizációjú diszkriminatív tapintás, kinesztézia (tér- és időbeli mintázat) Durva lokalizációjú tapintás 28. ábra A hátsó köteglemniscus medialis rendszer és az általa közvetített modalitások (tapintás/nyomás, „lebegés”/vibráció). Figyeljük, meg, hogy tapintási információ (durva) az AL-rendszerben is reprezentált, így csak nagyon kiterjed gerincvelői sérülés esetén van teljes taktilis kiesés 31 Agykéreg Cerebellum Thalamus ATAXIA: A kisagy proprioceptív Hátsó köteg bemenete hiányzik Hátsó köteg Anterolaterális köteg magvak Receptorok:
izomorsó inorsó bőr mechanoreceptorok 29. ábra A hátsó köteglemniscus medialis rendszer és az általa közvetített modalitások (propriocepció). A felszálló kapcsolatok a propriocepció gnosztikus feldolgozását szolgálja, míg a szegmentális és interszegmentális kapcsolatok a reflexes mozgáskoordináció szolgálatában állnak 32 a thalamus-ban „kapja meg”, ahol a trigeminális rendszer által összegyűjtött szenzoros információ egyesül a HK–LM- rendszer területéről származó afferentációval. A HK–LM-rendszerben aszcendáló jelek thalamikus átkapcsolódását precíz szomatotópia jellemzi. A fej területéről származó információ dominánsan a VPM thalami-ba, míg a test egyéb területeiről a VPL thalami-ba vetülnek a n. trigeminus illetve a lemniscus medialis szekunder afferensei. A legkaudálisabb területek a VPL thalami laterális részébe, a váll és kéz a VPL thalami mediális részébe, a kéz proximális része a VPM
thalami laterális részébe, míg a fej a VPM thalamiba, a száj körüli részek és a száj nyálkahártyája a VMP thalami legmediálisabb területére vetül. A thalamikus neuronok receptív mezője kisméretű, vagy a primer vagy a szekunder neuronénak felel meg és a rendszer kereszteződése miatt az ellenoldali testfélre lokalizáltak. A HK–LM-rendszer jeleinek kérgi projekciója és feldolgozása a thalamus VPL és VPM specifikus magjaiból az agykéreg primer szenzoros areájába (SI) történik oly módon, hogy a thalamus szintjéig megtartott szomatotópia megmarad, és egyben a reprezentált modalitásoknak megfelelően megnégyszereződik. A szigorú szomatotópia ellenére az agykérgi működés plaszticitást mutat, sérülés esetén képes a funkciók bizonyos mértékű átrendezésére, a kiesett funkciók helyettesítésére. Az SI kérget négy Brodmann-area alkotja (30. ábra), melyben az egyes modalitások dominanciája különböző: 3a –
izomorsó afferensek, 3b – tapintás, 1 – gyorsan adaptálódó felületes receptorok, 2 – izületekre bontott mélyérzés. A feldolgozás a 3a– 3b–1–2 sorrendben egyre komplexebb. Mindegyik Brodmann-areának saját homunculusa van. A kérgi szenzoros homunculus arányai tükrözik azt a sejtarányt, melyet az adott kérgi szenzoros area neuronális pool-ja az ellenoldali megfelelő testtájból származó szenzoros információ feldolgozásának szentel. Ez az arány igen nagy a száj és környékére vonatkozóan, a kéz ujjainak megfelelően, de például igen alacsony a hátnak megfelelően. Vegyük észre, hogy a thalamikus specifikus projekció nem csak a homunculus-szal jellemezhető térbeli elrendeződést mutatja, hanem egy bőr (felületi – taktilis) és izom (mély – prorioceptív) irányút is, mely szerint a thalamus kérgi részébe vetült izmokból és ízületekből származó proprioceptív és mélyérzési afferentáció az SI perifériájára
(Br. 3a és 2), míg a thalamus magjába vetült bőrből származó taktilis afferentáció az SI centrumába (Br. 3b és 1) jut 33 PRIMER MOTOROS AREA PRIMER SZENZOROS AREA 1 4 2 izületekre bontott mélyérzés 3b 3a Köpeny (izomokból, ízületekből ⇒ propriocepció) A kézizomzat szenzoros és motoros innervációja szorosan integrált izomafferensek THALAMUS Mag (bőrből ⇒ taktilis érzékelés) 30. ábra A hátsó köteg – lemniscus medialis rendszer által közvetített modalitások thalamocorticalis projekciója a primer szenzoros areába. A szenzoros homunculusszal jellemzett topológia mellett nagymértékű funkcionalitás jellemzi a projekció topológiáját. Pl a kéz izomzatának szenzoros (Br 3a) és motoros (Br 4) innervációja szomszédos területekre lokalizált. (Berne and Levy, Physiology, Fourth Edition, Fig 8-12 alapján.) Modalitás X Modalitás Y Gátló udvar Modalitás Z 0,5 mm 31. ábra Az agykérgi szenzoros jelfeldolgozás
kolumnáris organizációja. Vázlatosan három kolumna látható az agykéreg felszínére vetítve. A kolumnák modalitás-specifikusak Központjukat gátló udvar veszi körül. 34 (30. ábra) A primer areát egy másodlagos, még összetettebb feldolgozást végző terület (SII) határolja. Az agykérgi jelfeldolgozást a kolumnáris organizáció jellemzi Ennek lényege, hogy kb. tízezer neuron az agy felszínére merőleges kb 0,5 mm átmérőjű oszlopokba rendeződik, és egymással szoros kapcsolatot alakít ki egy szubmodalitás meghatározására, analízisére a test egy pontjára vonatkozóan. Az agy felszínét a nagyszámú kolumna mozaikszerűen borítja be. A kolumnák által analizált modalitások keverednek, így az egyes kolumnák közötti szomszédos kapcsolatok kialakításával egyre komplexebb analízisre nyílik lehetőség (31. ábra) Ezért a kolumnáris szerveződés alkalmas összetett tulajdonságok jelenlétének jelzésére
(tulajdonság-detektor, majomkísérletes példa: egy kolumna leadása akkor volt maximális, ha a tenyeret egy taktilis ingersorozat diagonális irányban, a csukló ulnáris részétől a mutatóujj tövének irányában érte). A specifikus thalamikus afferentáció a kolumna IV. rétegébe érkezik és a II, III, V és VI rétegekből lép ki a kolumnáris feldolgozás végeredményét képező jelsorozat, és halad a szomszédos vagy távolabbi kolumnák felé, ahol a feldolgozása már más szempontok szerint tovább folyatódik. Az SI régió funkcionális jellemzésére legmegfelelőbb, ha felsoroljuk, hogy milyen kiesésekkel kell számolnunk az SI-régió teljes pusztulásakor (vagy műtéti eltávolításakor). • A szomatotópia szerinti kiesések jellemzőek, de plaszticitás is van! • SII kiesése nincs hatással SI-re, mert sorbakapcsoltak. • A személy nem tudja lokalizálni a finom, diszkriminatív taktilis inger forrását. Meg tudja ugyanakkor határozni,
hogy mely végtagon, nagyobb testtájon történik az ingerlés, jelezve ezzel, hogy a szubkortikális központok bizonyos mértékű lokalizációra képesek. • A személy nem tudja meghatározni a bőrét ért nyomás mértékét. • A személy nem tudja meghatározni a tárgyak súlyát. • A személy nem tudja meghatározni a tárgyak alakját, formáját (stereognosis hiánya), illetve nem ismeri fel a bőrére írt betűket, jeleket (graphesthesia hiánya). • A személy nem tudja megítélni egy általa megérintett, végigsimított felület anyagi minőségét, ugyanis ehhez a finom taktilis ingereket közvetítő bőr mechanoreceptorokból származó jelek komplex kérgi feldolgozása szükséges. • Mivel a HK–LM-rendszerben a hő- és fájdalomérzet nem reprezentált, ezért a hő- és fájdalomérzet megtartott, de a személy nem tudja kritikusan értékelni és lokalizálni ezeket a modalitásokat. Az anterolaterális rendszer és a fájdalom
fiziológiája: 35 • Kizárólag posztszinaptikus rostok alkotják • Kontralaterálisan a VPL thalami-ba vetülnek • Bilaterálisan a formatio reticularis-ba vetülnek • Fő pályája a tr. spinothalamicus • Modalitások: nocicepció (fájdalom), hőérzés, durva tapintás • Rostjai lehetnek gyors vezetésűek és modalitásspecifikusak, vagy lassúak és polimodálisak • Nagyon sok a viszcerális impulzus (Head-zónák, szomatoviszcerális kapcsolatok) • NINCS specifikus agykérgi projekciója A tr. spinothalamicus sejtjei két csoportba sorolhatók Az egyik csoport ingerküszöbe alacsony, sokféle ingerre érzékenyek (polimodálisak, aspecifikusak) és válaszuk arányos az ingerintenzitással, annak széles tartományában (széles dinamikus tartományúak). Az aspecifikus sejteken sok mechano- és nociceptor konvergál A gyenge ingerrel kiváltott válaszukat a magasabb központok blokkolják. Ha ez nem következik be, akkor már enyhe
mechanikus ingerek is fájdalmat váltanak ki (mechanikus allodynia). A másik csoportot azok a sejtek alkotják, melyek ingerküszöbe magas, csak specifikus nociceptív ingerekre válaszolnak. Az anterolaterális rendszer által közvetített fájdalom biológiailag és így klinikailag is nagyon jelentős modalitás. A tr spinothalamicus kétféle rostkontingenst tartalmaz, mely az akut illetve a krónikus fájdalom közvetítéséért felelős (IV. Táblázat) IV. Táblázat A pálya neve Tr. Paleospinothalamicus Tr. Neospinothalamicus Vezetési sebesség lassú (C) gyors (Aδ) Modalitás specificitás polimodális specifikus Thalamikus projekció nem specifikus magvak specifikus magvak A thal. projekció jellege diffúz lokalizált Precíz kérgi lokalizácó nincs A fájdalom jellege késői, tompa, erős, diffúz Kiváltott reflexek antalgiás, kímélő tartás, vegetatív tünetek 36 lokalizáció és mennyiségi kiértékelés a kéregben korai, éles
menekülési reflexek A fájdalomérzet kialakulásához nem szükséges az agykéreg! Az agykéreg a fájdalmi információ diszkriminatív, értelmező feldolgozását végzi. A thalamus működése adja a fájdalom eredendően negatív emocionális töltését. Így érthető, hogy a thalamus sérülése (pl. agyvérzés) esetén az ellenkező testfélre lokalizált, rendkívül heves, kellemetlen jellegű, fájdalmas állapot kialakulását eredményezheti tényleges fájdalmas inger jelenléte nélkül (thalamus szindróma, centrális fájdalom). A frontális lebeny határozza meg, hogy a fájdalom mennyire kellemetlen, és hogy mennyire zavarja a beteget. Ezért, különösképpen a fájdalom gyógyszeres befolyásolhatóságának hiányában, korábban a prefrontális lobektómia hasznosnak bizonyult igen erős fájdalmak (pl. rákos betegség) csillapítására (A fájdalom sebészi csillapításának egy másik sebészi eljárása az anterolaterális cordotomia,
mikor is a tr. spinothalamicus lateralis rostjait vágják át, általában a ventrális tapintási információt közvetítő rostok épen hagyásával. Ha ezek mégis átvágásra kerülnének, taktilis kiesés mégsem tapasztalható, hiszen a HK–LM-rendszer intakt marad.) Viszcerális eredetű fájdalom gyakran sugárzik bőrfelszínünk tipikus régióiba. Ennek oka az, hogy a gerincvelő szegmentális elvet követve fejlődik, és emiatt úgy a szenzoros, mint a motoros innerváció szegmentális jellegű (Head-zónák). Egy szegmens által beidegzett bőrterületről (dermatóma) származó afferens rost, és az adott szegmens által innervált zsigeri terület afferentációja egyazon gerincvelői neuronra konvergál, és így a zsigeri eredetű fájdalom az adott dermatómára vonatkoztatva tudatosul. Egy másik lehetőség az, ha egy facilitált állapotban lévő szomatikus neuronnal szinaptizáló viszcerális kollaterális idézi elő a szomatikus neuron válaszát. A
sugárzó fájdalom klinikai jelentősége nagy, hiszen felhívja az orvos figyelmét a potenciálisan súlyos következményekkel járó viszcerális kórfolyamatra (pl. a szívizom csökkent véráramlásával járó állapotában fájdalom jelentkezhet a bal vállban és karban). Egy végtag elvesztése, vagy műtéti eltávolítása után – annak ellenére, hogy a sebgyógyulás és a szöveti regeneráció már befejeződött – fájdalmas inger hiányában is fájdalom jelentkezhet, melyet a beteg az elvesztett végtagba lokalizál (fantomfájdalom). Látható, hogy a fájdalom észlelése egy igen kiterjedt neurális rendszer integrált működéséhez kötött. Ha a rendszer egyes elemei kiesnek vagy kapcsolatukban zavar támad, az egy kóros természetű, adott esetben igen intenzív fájdalom kialakulásához vezethet, melynek csillapítása nagyon nehéz. 37 Intenzív fájdalommal járó állapotok működésbe hozzák az endogén analgetikus rendszert, mely
átmeneti időre a fájdalmat hatékonyan képes csökkenteni, és így lehetőséget ad a fájdalmas ingertől való eltávolodásra. A rendszer vertikálisan szervezett gátló neuronokból áll. Kiindulási helye a periaqueductalis magvak, és támadáspontja a fájdalmi ingerület gerincvelői színtű elsődleges átkapcsolódása (32. ábra). A rendszer endogén stimulánsai az endogén ópiátok (enkefalinok, endorphinok, dynorphin), melyek a µ, δ és κ ópiát receptorok természetes ligandjai. Az orvosi praxisban leggyakrabban használt természetes ópiát a morfium, egy igen erős kábítószer, melyhez azonban az endogén ópiátokkal szemben, gyakran alakul ki végzetes jellegű gyógyszerfüggőség. Használata súlyos, szenvedéssel járó esetekben elkerülhetetlen. Az endogén analgetikus rendszer működése a primer fájdalmi ingerület gerincvelői mediációjának pre- és posztszinaptikus gátlására irányul (33. ábra). A rendszert alkotó gátló neuronok
ingerületi állapota a rendszer inaktív és aktív állapotaiban a 34. ábra szerint változik A rendszer inaktív állapotában a GABAerg neuronok tónusos gátlás alatt tartják a leszálló analgetikus pályát. A pálya egymást követő gátló neuronjainak működése az aktív (+) – inaktív (-) funkcionális állapotok szerint ismétlődik. Ennek végeredményeként a gerincvelői szinten az opiát neuronok gátolt állapotba kerülnek, tehát nincs analgézia. Morfin vagy endogén opitátok a rendszert annak eredeténél és a gerincvelői szinten hozzák működésbe, az előbbi esetben a GABAerg neuronok aktivitásának felfüggesztésével, az utóbbiban a nociceptív átkapcsolódás pre- és posztszinaptikus gátlásával. Mindkét hatás analgéziát eredményez. Az endogén analgetikus rendszer hatékonyságát jól jellemzik a harctéri vagy trauma-helyzetekben leírt esetek, amikor a súlyos traumát szenvedett egyén addig nem érzett fájdalmat, míg a
fájdalmat előidéző veszélyhelyzet el nem múlt, azt meg nem szokta, vagy segítség nem érkezett. Ekkor ugyanis a fájdalom előidézte felfokozott idegrendszeri állapot (stress analgézia) – mely endogén opiátokat szabadít fel – csökken, és így a rendszer inaktív állapotba kerül. 38 MORFIN OPIOID GÁTLÓ NEURON Periaq. magvak GABAERG GÁTLÓ NEURON MONOAMINERG GÁTLÓ NEURON Medulla MORFIN Gerincvelő Gátló mechanizmus 32. ábra A fájdalom endogén szupresszióját végző analgetikus rendszer szerkezete. A rendszer vertikálisan kapcsolódó gátló neuronokból áll. A leszálló rendszer támadáspontja a nociceptív ingerületek első gerincvelői átkapcsolódása. A folyamat vagy endogén, vagy exogén opiát ligandokkal stimulálható. (Fonyó, Az orvosi élettan tankönyve, második kiadás, 37-6. ábra alapján) 39 Opioid gátló interneuron Morfin (alsó) Pre- posztszinaptikus gátlás 33. ábra A gerincvelői nociceptív
mechanizmusának sémája átkacsolódás GÁTLÓ NEURONOK ÁLLAPOTOK Aktív (gátol) pre- és RENDSZER INAKTÍV posztszinaptikus gátló RENDSZER AKTÍV Opiát 1 Blokkolt Monoaminerg 2 + Tónusos gátlás Nem blokkolt Monoaminerg 1 Tónusos gátlás GABAerg Inaktív (nem gátol) Opiát 2 Gerincvelői átkapcsolódás NINCS ANALGÉZIA ANALGÉZIA 34. ábra Az endogén analgetikus rendszer inaktív és aktív állapotát jellemző funkcionális kapcsolatok 40 HK–LM-RENDSZER ANTEROLATERALIS RENDSZER Szinoním elnevezések • Specifikus • Epikritikus • Gnosztikus Klinikai alapon Szinoním elnevezések • Nem specifikus • Protopátiás • Hő- és fájdalomérzés Gyors Vezetés Precíz Megtarott Kis receptív mezők ARAS Lassú Diffúz Nagyfokú konvergencia és divergencia Szomatotópia neo- 1:1 SPECIFIKUS ASSZOCIÁCIÓS MAGVAK (Mediális, középvonali, pulvinar, reticularis) INT paleo- THALAMUS SPECIFIKUS MAGVAK (VPL [törzs,
végtagok] VPM [arc, fej] VL [xlat kisagy, ncl. ruber]) NEM SPECIFIKUS (DIFFÚZ) MAGVAK INT INT ASP (Ventr. ant, intralaminaris, középvonali) ASP 1:1 ARAS INT ASP AGYKÉREG ALATTI RÉGIÓK AGYKÉREG SPECIFIKUS KÉRGI ZÓNÁK (Szomatoszenzoros, szomatomotoros, halló-, látó-, Br. 3,2,1 [törzs, végtagok,arc,fej] Br. 4,6 [xlat kisagy, ncl ruber]) ASSZOCIÁCIÓS KÉRGI ZÓNÁK (A primer zónákkal szomszédos területek) 35. ábra A szomatoszenzórium szerkezete és az alkotóelemek közötti kapcsolatrendszer. ARAS = Aszcendáló Retikuláris Aktiváló Szisztéma, INT = integráló kapcsolat, ASP = aspecifikus kapcsolat. 41 AGYI ELEKTROMOS TEVÉKENYSÉG Az agy működése elektromos tevékenységének regisztrálásával követhető. Tanulmányozása jelentős segítséget nyújtott az agyi szenzoros, motoros és mentális tevékenység jobb megértéséhez. Az elektromos tevékenységet regisztrálhatjuk a fejbőrre helyezett elektródokkal, vagy az agy
felszínén (field- vagy mező-potenciál) illetve intracelluláris elektródákkal (unit- vagy egység-potenciál). Az agykérgi kiváltott potenciálok Az agykéregbe érkező szenzoros jel az agykéreg felszínén átmeneti potenciálváltozást hoz létre, melyet a kérgi felszín alatti denritek posztszinaptikus potenciáljainak összegződése, és nem a beérkező szenzoros AP-ok hoznak létre. Izolált primer kiváltott potenciált a primer szenzoros kéregterület felett lehet regisztrálni (36. ábra) Ez a szomatotopikus jel alkalmas az agykéreg szenzoros feltérképezésére. Kiváltott potenciál a primer területek környezetéből, illetve ettől távolabb is elvezethető (másodlagos kiváltott potenciál), melyet azonban nem a primer potenciál intrakortikális terjedése, hanem thalamikus aspecifikus projekciók hoznak létre. A másodlagos kiváltott potenciál lassúbb lefolyású, mint az elsődleges és így az elsődleges mintegy beleolvad annak kezdeti
fázisába (36. ábra) A kiváltott potenciálok az EEG-jelekkel azonos nagyságrendű és – kialakulási mechanizmusukat tekintve is – hasonló jelek. Mivel beleolvadnak a zajszerű EEG-jelbe, ezért csak jelátlagolási módszerekkel regisztrálhatók olyan tisztán, mint azt a 36. ábrán látjuk Az EEG Az agy nem csak specifikus afferentációval kiváltható elektromos válaszra képes, hanem folyamatos, „spontán” elektromos aktivitást is mutat, melyet a fülcimpához, mint referenciához viszonyítva a hajas fejbőrre helyezett elektródákkal, és kellően nagy erősítéssel regisztrálni lehet 42 (elektroenkefalográfia, EEG). A feszültségingadozások nagyságrendje µV-os (!), tehát nem tévesztendő össze a biológiai membránok mV-os nagyságrendű nyugalmi vagy akciós potenciáljának PRIMER KIVÁLTOTT POTENCIÁL (izolált, szomatotopikus) SZEKUNDER KIVÁLTOTT POTENCIÁL (kiterjedtebb, nem szomatotopikus) 200 µV Primer szenzoros kégi locus
Primer kezdeti rész + 100 ms 36. ábra Primer és szekunder agykérgi kiváltott potenciálok. (Ganong, Review of Medical Physiology, Fourteenth Edition, Fig. 11-4 és Bálint, Orvosi élettan, 1986, 94/1 ábra alapján.) 43 nagyságrendjével. Egy-egy elektróda több ezer kolumna aktivitását regisztrálja A hullámokat görög betűvel jelöljük. Az EEG-hullámok amplitúdója és frekvenciája az agy funkcionális állapotával változik (V. Táblázat) Minél kisebb az agyi működés éberségi szintje, annál szinkronizáltabb az agyi elektromos tevékenység, annál nagyobb az amplitúdó és kisebb a frekvencia. Nagyon nagy amplitúdójú hullámtevékenység kóros, és jelzi, hogy igen nagy agykérgi területekre terjed ki a normálisnál nagyobb mérvű szinkronizáció. Ezek a hullámok általában egyes EEGelvezésekben, tehát fokálisan mutatkoznak (epilepsziás görcsök) V. Táblázat EEG-hullám Normalizált amplitúdó Frekvencia (Hz) Állapot
intenzív figyelem vagy γ 0,5x (?) 30-50 β 1x 14 felett éber α ~2x 8-13 nyugalom, felületes alvás θ ~3x 4-7 közepesen mély alvás δ ~5x 0,5-3 mély alvás ~10x ~3, változó epilepsziás görcs REM-alvás Az EEG eredete Az EEG-ben tükröződő agyi elektromos tevékenység nem az agykérgi neuronok akciós potenciál sorozatainak összege. Eredete a thalamusból az agykéreg felső rétegeibe érkező aspecifikus projekció által kialakított dipólusokban keresendő, melyek az agykéregben a felszínre merőleges irányú, passzív extracelluláris ionáramokat keltenek. Az így létrejövő, alapvetően dentritikus poteciálokat rögzíti az EEG (37 ábra). 44 I. Dendritikus arborizáció II. III. Aspecifikus thalamikus afferentáció IV. V. Piramissejt test VI. ++++ EC-áram + + + + + + Aspecifikus thalamikus afferentáció 37. ábra A thalamicus aspecifikus afferenctáció és a piramissejtek kapcsolata az
agykéreg felszíni rétegeiben. Anatómiai viszonyok az ábra felső részén láthatók A piramissejt dendritjeit depolarizálja a thalamikus aspecifikus afferentáció így kialakítva egy kérgi dipólust a kérgi szinapszisok és az V. rétegben lévő piramis sejttestek között (szaggatott vonal) Az EEG-ben regisztrált feszültséget a kéreg felszínére merőlegesen folyó passzív extracelluláris áramok hozzák létre. (Ganong, Review of Medical Physiology, Fourteenth Edition, Fig 11-2 és Fonyó, Az orvosi élettan tankönyve, második kiadás, 38-2. ábra alapján) 45 Az „ébresztőrendszer” (Aszcendáló Retikularis Aktiváló Szisztéma) és az EEG deszinkronizációja A nyúltagytól az agytörzsön és a hídon át a hypothalamus környékéig hatalmas, poliszinaptikus neuronális kapcsolatban lévő idegsejt populáció, a formatio reticularis helyezkedik el. Ezekhez a neuronokhoz minden aszcendáló szenzoros pálya kollaterálisokat ad (35. ábra) A
kollaterálisokon beérkező jelek a nagyszámú poliszinaptikus kapcsolódás során felerősödnek, és a jelentős konvergencia miatt elvesztik modalitás-specificitásukat. Az aspecifikus neuronális információ (ASP 35 ábra) vagy a thalamus aspecifikus magvain átcsatolódva, vagy a thalamust megkerülve jut az agykéregbe. Ez a kérgi projekció diffúz, kiterjed minden kérgi területre. Szerepe az agy ébresztésében és a szenzoros információ feldolgozását elősegítő intenzív koncentráció fenntartásában van. Az ARAS működése nélkül az agykéreg szenzoros funkcióit nem tudja megvalósítani, ténylegesen alvó állapotba kerül. Az ARAS aktivitása az EEG-t deszikronizálja, tehát az EEG-jelek amplitúdóját csökkenti, és frekvenciáját növeli (VI. Táblázat) VI. Táblázat RELÉ (ÁTKAPCSOLÓ) Üzemmód (deszinkronizáló) DESZINKRONIZÁLT EEG-regisztrátum Tudati állapot ARAS Thalamocorticalis sejtek nyugalmi potenciálja ÉBER BE DEPOLARIZÁLT
OSZCILLÁTOR (szinkronizáló) SZINKRONIZÁLT Üzemmód EEG-regisztrátum Tudati állapot ARAS Thalamocorticalis sejtek nyugalmi potenciálja ALVÓ KI HYPERPOLARIZÁLT 46 Az EEG szinkronizációja Az a tény, hogy a több milliméternyi EEG-elektróda által „látott” több ezer piramissejt szummált dendritikus potenciáljai 0 µV-tól – azaz az izoelektromos szinttől – eltérő, formált EEG-hullámokat eredményez, azt jelenti, hogy számos agykérgi kolumna aktivitása egymással szinkron, potenciáljaik azonos fázisba kerülnek. A szinkronizáló nem specifikus afferentációt nagyrészt a thalamus tartja fenn (VI. Táblázat) A mechanizmus alapját azok a visszacsatoló körök képezik, melyeken keresztül egy, a thalamus nem specifikus magvaiból a kérgi piramissejtek dendritjeihez futó aspecifikus afferentáció egyben gátolja a projiciáló, illetve a szomszédos sejtek aktivitását. Ezek a sejtek a mintegy 100 msec-ig tartó gátlás után felszabadulva
aktív állapotba mennek át. A thalamicus oszcillátor frekvenciája függ a beérkező szenzoros ingerületektől, valamint az ébresztés szintjétől, és érzékeny a narkózisra is. 50 Hz specifikus szenzoros ingerlési frekvencia felett megszűnik az agykérgi dendritikus IPSP–EPSP-ciklus, és így az agykérgi lassú hullámú tevékenység deszinkronizálódik (átmenet az α-ritmusból a β-ritmusba). A thalamus és az agykéreg kapcsolatát jellemzi, hogy • A thalamus és az agykéreg reciprok neuronális kapcsolatban vannak. • A thalamus ritmikus aktivitása EPSP–IPSP-ciklusokat gerjeszt az agykéregben, mely szinkronizált kérgi EEG-hullámokká (α) integrálódik. • A thalamus ritmikus aktivitása az éberségi szint függvénye. • A thalamus egy kapu: ha átengedi a specifikus aszcendáló szenzoros információt, akkor egyben lehetővé teszi, hogy a kéreg azt befogadja (VI. Táblázat, RELÉ-üzemmód); ha nem, akkor a szinkronizált szerveződés
állapotában biztosítja, hogy a kéreg feldolgozhassa a korábban befogadott információt (VI. Táblázat, OSZCILLÁLÓ-üzemmód) Ébrenlét, alvás, cirkadián ritmus Az agykéreg működése nélkül nincs éber, tudatos tevékenység kivitelezésére alkalmas állapot. De láttuk, hogy az ARAS, valamint a thalamus milyen fontos szerepet játszik az agykérgi aktivitásnak az aktuális szenzoros affrerentációs szinthez történő 47 hangolásában. Megnövekedett, változatos szenzoros afferentáció, illetve ARASaktivitás az EEG deszinkronizációjához vezet, mely az éber állapot elektrofiziológia jele is egyben. A szenzoros afferentáció alacsonyabb szintje csökkenti az ARAS által kibocsátott aspecifikus neuronális efferens aktivitást, illetve csökkenő frekvencia mellett növeli a thalamus szinkronizációját. Mindez hasonló természetű változásokat idéz elő az EEG-ben is. Az éber állapottól a mély alvásig fokozatosan nő az EEGjelek
szinkronizációja (amplitúdó nő, frekvencia csökken) és csökken az éberségi szint (39. és 40 ábra) Az alvási orsók megjelenése egybeesik a tudatos percepció megszűnésével. Az alvás alatt a szinkronizáció mértéke oszcillál (V Táblázat, 41 ábra). A szinkronizáció mértéke, és így az alvás mélysége elalvás után kb 45 perc múlva a legmélyebb, majd 4-5 egyre kisebb mélységű cikluson keresztül a reggeli felébredésig ismétlődik. Idegrendszeri és testi működésünk az alvás során két, egymástól jelentősen eltérő állapotot mutat. Az egyik gyors szemmozgással (Rapid Eye Movement) párosul, ezért REM-alvásként, a másikat NREM-alvásként (Nem REM) említjük. Az NREM-alvási stádiumokban az alvás mélysége ciklusosan változik. Az izomtónus sosem szűnik meg, így az alvó időről időre változtatja testhelyzetét. Az NREM-alvás felületes stádiumában (és csakis ekkor!) az NREMalvás átvált a REM-alvásba (41 ábra) Ebben
a fázisban az alvó nehezen ébreszthető, bár spontán ébredés a felületes NREM-alvási stádiumban gyakori. A legjellemzőbb a gyors szemmozgás, az EEG deszinkronizálódik, az izomtónus (kivéve a szem-, középfül- és légzőizmokat) megszűnik. Jelentős vegetatív változások tapasztalhatók: a vér adrenalinszintje, a szívfrekvencia és a vérnyomás emelkedik, a nemiszervek véráramlása fokozódik (erekció). Ebben a fázisban intenzív az álomtevékenység, de az izomtónus hiánya miatt az álomképek motoros aspektusai nem kerülnek kivitelezésre. A REM-alvásból felébresztettek „szenzoros” jellegű álmokról számolnak be, míg az NREM-alvásra inkább a „gondolati” jellegű álmok jellemzőek. A naponta alvással töltött idő és a REM/NREM arány az élet során változik (42. ábra). Az elalvást nem az ARAS inaktiválódása idézi elő. Az alvás aktív folyamat Lassú hullámú alvás központ • a medulla középvonalában a raphe
magvakat is magában foglalva • szerotonin mediáció • léziója álmatlanságot okoz 48 ÁLLAPOT STILIZÁLT EEG-HULLÁMOK EEG-HULLÁM Éber β Nyugalom, felületes alvás α Alvási orsó Közepesen mély alvás θ δ Mély alvás 0 1 2 Idő (sec) 3 4 39. ábra Az EEG frekvenciájának és amplitudójának változása az ébrenlét-alvás ciklus kapcsán. (Bullock, Boyle III, Wang, NMS Physiology, Third Edition, Fig. 8-1 alapján) Éber Nyugalom Álmos Alvás – 2. stádium Alvás – 4. stádium 50 µV 1 sec 40. ábra Alváslaboratóriumban készült eredeti EEG-regisztrátumok 49 Átmeneti Átmene éber tiperiódusok éber Végleges ébredés REM-alvás Éber Felületes . Közepesen mély . Mély 0 1 2 3 4 5 6 IDŐ (óra) 41. ábra Az alvási stádiumok ciklikus váltakozása egy éjszaka folyamán. Mély alvásból és REM (Rapid Eye Movement)-alvásból egyaránt nehéz felébreszteni az alvót. Az éjszaka folyamán rövid
időszakokra az EEG ébredés jelét mutatja. Az alvásból történő végleges ébredésre az egyre felületesebbé váló alvási ciklusok vezetnek. (Bullock, Boyle III, Wang, NMS Physiology, Third Edition, Fig. 8-2 alapján) 100 % ALVÁS % 25 % REM % kora- új- csecsemő gyermek pubertás szülött felnőtt öreg ÉLETKOR 42. ábra Az alvás aránya a nap százalékában és a REM-alvás aránya az alvással töltött idő százalékában kifejezve az életkor függvényében 50 REM-központ • híd fomatio reticularis a locus ceruleust is magában foglalva • noradrenalin mediáció • léziója kiiktatja a REM-fázisokat Alvásra a szervezetünknek mindenképpen szüksége van. Az alváshiány destabilizálja a mentális és vegetatív funkciókat. Az alvás végleges meggátlása a szabályozási mechanizmusok széthullása miatt halálhoz vezet. Az alváshiányt szervezetünk bepótolja. Az alvási zavarok – mint pl a narkolepszia (hirtelen fellépő
REM-alvás), a katalepszia (mint előbb, de eszméletvesztés nincs), az alvajárás, ágybavizelés (gyermekeknél gyakori), rémálmok – gyógyítása fontos betegségmegelőző illetve terápiás tevékenység. Az ébrenlét–alvási ciklus periódusidejét endogén tényezők (a két nucleus suprachiasmaticus aktivitása) határozzák meg. Az endogén ciklus hosszabb, mint a 24 órás napi ciklus (cirkadián ritmus). A két suprachiasmaticus mag retinális kapcsolatai révén (retinohypothalamicus pálya) hangolja az endogén ébrenlét–alvási ritmust a nappalok és éjszakák váltakozásának 24 órás üteméhez, melyben a retinából származó fényingereknek döntő szerepe van. Emberben emellett még egyéb hatások is befolyásolják az ébrenléti és alvási periódusok hosszát. Napi ritmusban nem csak az ébrenlét, hanem a szervezet számos más funkciója is mutat periódikus változást (testhőmérséklet, hormonszintek stb.) 51 FELHASZNÁLT FORRÁSOK
Bálint, P.: Orvosi élettan, Medicina, 1986 Berne, R. M; Levy, M N; Koeppen, B M; Stanton, B A: Physiology, Fourth Edition, Mosby, 1998. Bullock, J.; Boyle, J III; Wang, M B: National Medical Series (NMS), Physiology, Third Edition, Williams and Wilkins, 1995. Fonyó, A.: Az orvosi élettan tankönyve, második kiadás, Medicina, 1999 Ganong, W. F: Review of Medical Physiology, Fourteenth Edition, Prentice-Hall international Inc., 1989 Guyton, A. C; Hall, J E: Textbook of Medical Physiology, Ninth Edition, W B Saunders Company, 1996. Silbernagl, S.; Despopoulos, A: SH atlasz Élettan, Springer Hungarica, 1994 52