Comments
No comments yet. You can be the first!
Most popular documents in this category
Content extract
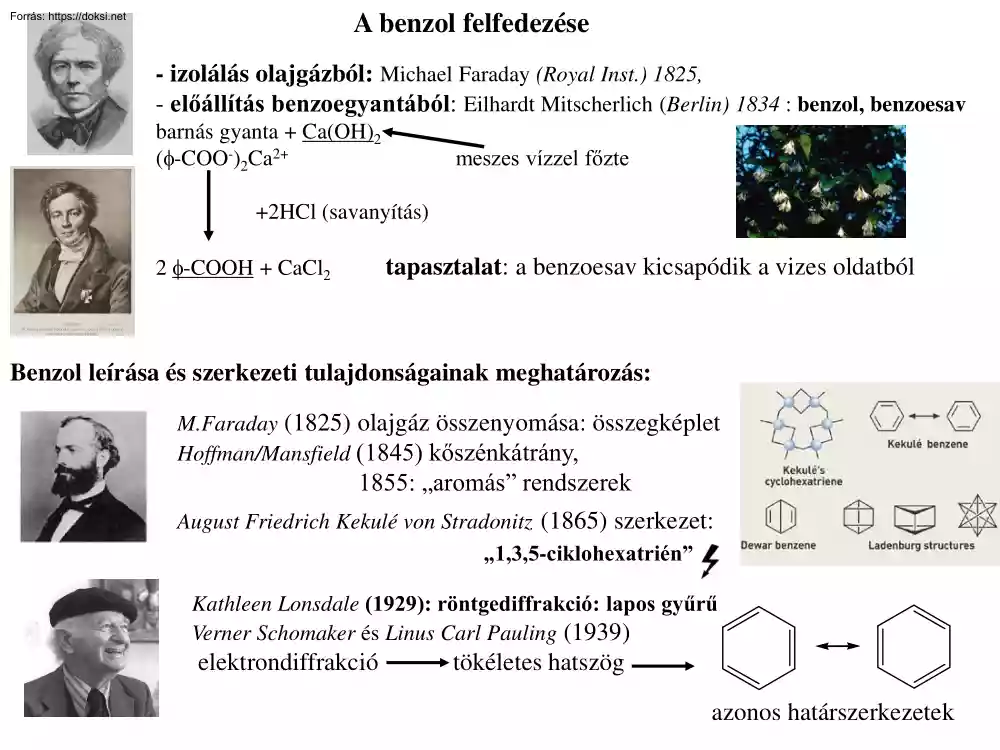
A benzol felfedezése - izolálás olajgázból: Michael Faraday (Royal Inst.) 1825, - előállítás benzoegyantából: Eilhardt Mitscherlich (Berlin) 1834 : benzol, benzoesav barnás gyanta + Ca(OH)2 (-COO-)2Ca2+ meszes vízzel főzte +2HCl (savanyítás) 2 -COOH + CaCl2 tapasztalat: a benzoesav kicsapódik a vizes oldatból Benzol leírása és szerkezeti tulajdonságainak meghatározás: M.Faraday (1825) olajgáz összenyomása: összegképlet Hoffman/Mansfield (1845) kőszénkátrány, 1855: „aromás” rendszerek August Friedrich Kekulé von Stradonitz (1865) szerkezet: „1,3,5-ciklohexatrién” Kathleen Lonsdale (1929): röntgediffrakció: lapos gyűrű Verner Schomaker és Linus Carl Pauling (1939) elektrondiffrakció tökéletes hatszög azonos határszerkezetek A benzol térszerkezete: memo: d(CC)=1.48Å, d(C=C)=134Å d(C-H)=1.098Å d(C-C)=1.397Å a(CCC) =120o w(CCCC) =0o Benzol hatfogású szimmetriatengellyel rendelkező síkalkatú szimmetrikus
gyűrűs molekula. Minden C-atomja sp2-es hibridállapotú. A 6 db pz atom-pályából, 3 db p molekula pálya alakul ki: aromás elektronszerkezetű vegyület. „szokatlan” hogy nem mutatják a alkének tipikus addíciós reakciói Addició (cisz) H H OH KMnO4 / H2O KMnO4 / H2O H H Addició (transz) semmi OH H H Br Br2 / CCl4 Br2 / CCl4 H Br H Br Subsztitúció H Br Br2 / FeBr3 + HBr CCl4 Br H semmi „szokatlan” stabilitása: A jósolt -28.6 kcal/mol, vagy ennek többszöröse DH-hoz képest, a mért hidrogénezési „hő” jelentős stabilitásra utal: a rezonancia energia jelentős (-36 kcal/mol). A benzol tehát ugyancsak inert! + 3 H2 kat. / nyomás DH = -49.8(kcal/mol) H 3*ciklohexén = -85.8 rezonancia stab. = +360 D H (kcal/mol) 85.8 -36.0 57.2 -1.8 -57.4 28.6 -55.4 -49.8 -28.6 H 0.0 Wade 693 aromás rendszerek (szakkifejezéssé alakult): •delokalizált p-rendszer (alternáló egyes és kettős kötések): 4n+2 p-elektron
részvételével (4-el nem osztható; azok: antiaromás / nem-aromás) •síkalkat •gyűrűs VIII. Aromás szénhidrogének Homoaromás vegyületek: benzol, benzolrészekből felépülő molekulák és azok származékai, amelyek lehetnek monociklusos, policiklusos és kondenzált ciklusos szénhidrogének. Heteroaromás vegyületek:aromás elektronszerkezet S, N, és O atomokkal. 1. Monociklusos aromás szénhidrogének Két szubsztituens relatív helyzete: orto (1,2), meta (1,3) és para (1,4) Három szubsztituens relatív helyzete: vicinális (1,2,3), aszimmetrikus (1,2,4), és szimmetrikus (1,3,5) A. Telített oldalláncú monociklusos aromás szénhidrogének Típusnevek: Toluene toluol (metilbenzol) Benzene benzol E(RHF/6-311++Gd,p) CH3 CH3 karcinogén!!! piros kék -0.03 töltés 003 CH3 •xylos (görög): fa •petrolkémia CH3 CH3 = 0 Debye p-elektronszextett 1,2-dimetilbenzol (orto-xilol) o-Xylene CH3 1,3-dimetilbenzol (meta-xilol) m-Xylene CH3
1,4-dimetilbenzol (para-xilol) p-Xylene CH3 H3C CH3 H C CH3 CH H3C H3C CH3 mezitilén 1,3,5-trimetilbenzol mesitylene kumol izopropilbenzol Isopropylbenzene CH3 para-cimol 1-metil-4-izopropilbenzol p-Cymene Csoportnevek: H3C phenyl fenil- H 3C H3C o-tolyl o-tolil- p -tolyl p-tolil- m-tolyl m-tolil- CH3 nev. gyak H3C benzil- H3C H 2C 1 C H2 C C CH3 H2 21 4 H3C CH2 1-(1,1-Dimethylbutyl)-4-ethyl-2-methylbenzene 1-(1,1-dimetilbutil)-4-etil-2-metilbenzol Faj: ILLATOS AROMÁS VEGYÜLETEK Név: Vegyület: Mandula (Prunus amygdalus) keserűmandula benzaldehid Kömény (Cuminum cyminum) köményolaj o-, m- és p- cimol Kömény (Cuminum cyminum) köményolaj chuminaldehid (illatos folyadék) Fahéj (Cinnamomum zeylanicum) fahéjaldehid fahéjaldehid benzoefa gyantája (Styrax benzoin) benzoegyanta trópusi fa XVI. sz óta ismert tolulbalzsam benzoesav toluol kérdés: helyettesíthetünk-e egy aromás hidrogént egy alkil csoporttal?
válasz: igen, Friedel–Crafts-alkilezési (SE2) reakció során megvalosítás: pl. alkil-halogenid + Lewis-sav H CH3 AlCl3 CH Cl + HCl + CH3 2-klórpropán kumol izopropilbenzol általánosítás: más potenciális karbokationt eredményező reagens is alkalmas, pl. propén, ciklohexén Solomons 670, Bruckner II-125 kumol cikklohexilbenzol B. Telítetlen oldalláncú monociklusos aromás szénhidrogének helyzetizoméria H2C CH3 HC HC vinilbenzol sztirol vinylbenzene styrole H2C CH2 CH propenilbenzol propenylbenzene HC HC e (f Eth CH CH2 CH2 allilbenzol H2C allylbenzene HC 1,4-divinilbenzol p -divinilbenzol 1,4-Divinylbenzene CH C CH etinilbenzol (fenilacetilén) kat. Solomons 693 >10 milliárd kg/év 2. Izolált policiklusos aromás szénhidrogének Biphenyl bifenil H2C diphenylmethane difenilmetán memo: a két aromás gyűrű se nem koplanáris se nem merőleges (~40o) tetr tetr = 0 Debye C piros kék -0.033 töltés
0033 methane tán tetraphenylmethane tetrafenilmetán Csoportnevek: transz – op: 125C C sztilbén 1,2-diphenylethene C CH 1,2-dif eniletén CH tolán diphenylacetylene C CH sztilbén difenilacetilén 1,2-diphenylethene C CH 1,2-dif eniletén tolán diphenylacetylene difenilacetilén C cisz – op: 5-6C tritil- 3. Kondenzált policiklusos szénhidrogének feltétel: legalább két közös szénatom: - lineáris anelláció - anguláris anelláció memo: a naftalin kivételével mindegyik név „én” végződésű kétgyűrűs rendszerek: naftalin (szintelen) folytonosan konjugált (6+4 π-elektr.) aromás (=0D, 6- és 6-tagú gyűrűk) molyirtó naftalin (szintelen) Bruckner II 185 azonos azulén (mélykék határszerkezetek krist.) magnólia Bruckner II 1377 folytonosan konjugált (6+4 π-elektron = 4*2+2 ← aromás) szemiaromás (=1.1D, töltés szepar,7- és 5-tagú gyűrűk) azulén (mélykék krist.) nem-azonos határszerkezetek
nem-aromás rendszer Bruckner II 193 (6+2 π-elektr.) ( dipol, 6- és 5-tagú gyűrűk) memo: az aromás gyűrűhöz kondenzált ciklopentadién fokozott reaktivitású C H H 1H-Indene indén (szintelen folyad.) fokozott reaktivitású („savanyú”) metilén csop. (pl - indén + Na - indén + aldehid) C H Na 10 p-elektron = 4*2 + 2 ← aromás három gyűrűs rendszerek: 12 p-elektron ← nem-aromás bifenilén Biphenylene antracén Anthracene H2C fenantrén fluorén Phenanthrene 2-Methyl-3-vinyl-1H-indene kékesen fluoreszkáló szintelen tûkristály fokozott reaktivitású („savanyú”) C metilén csoport (pl. – fluorén + Na) H Na memo: a kialakuló anion esetében az aromacitás ki tud terjedni a mol. egészére 14 p-elektron = 4*3 + 2 ← aromás memo: A naftalin rezonancia energiája (-60 kcal/mol) kicsit alacsonyabb mint a benzol kétszerese (-36kcal/mol*2= -72kcal/mol). Az antracéné -84kcal/mol, míg a fenantréné -91 kcal/mol (-108 helyett).
négy és több gyűrűs rendszerek: naftacén krizén Naphthacene Chrysene naftacén krizén Naphthacene Chrysene perilén pirén Perylene Pyrene memo: megtalálhatók a dohányfüstben, a diesel autók fekete füstjében, perilén pirén Perylene Pyrene pentacén Pentacene koronén Coronene Példa: (a máj méregtelenítési stratégiája, reaktív intermedier, majd a vízoldhatóvá tétel glutationnal) e d c b f aril hidroxiláz (májban) O benzo[def ]krizén Benzo[def ]chrysene ez a ténylegesen karcinogén hatású vegyület Az teljes SCF elektronsűrűség alapján számított izo-felületek 0.004 0.02 perilén bronzsárga krist. (op 274oC) memo: 2 naftalin peri helyzetű összekapcsolódása 0.004 0.025 0.04 0.04 koronén sárga, krist. (op 429oC) hat benzolgyűrű körkörös anellációja, ciklikusan kondenzált gyűrűs aromás szénhidrogén aromaticitás – nem összefüggő p rendszerek IX. Aromás halogénezett szénhidrogének Egy
vagy több hidrogént X-re cserélünk halogénezés helye szerint:-magban szubsztituált (aril-halogenid), -oldalláncban szubsztituált (aral-kilhalogenid) Szn: előző fejezet alapneveiből (pl. benzol, fenantrén) képezzük (pl. jódbenzol, 9-brómfenantrén) Csn: előző fejezet csoportneveihez (pl. fenil, fenantril) tesszük a funkció nevet (pl klorid) és így kapjuk a (pl. fenil-jodid, fenantril-bromid) Cl diszubsztituált Cl monoszubsztituált Cl Cl Cl klórbenzol chlorobenzene Cl 1,2-diklórbenzol (o-diklórbenzol) 1,2-Dichlorobenzene Cl 1,3-diklórbenzol Cl Cl Cl (m-diklórbenzol Cl 1,3-Dichlorobenzene 1,4-diklórbenzol 1,2,4-triklórbenzol Cl (p -diklórbenzol) Cl 1,2,4-Trichlorobenzene 1,4-Dichlorobenzene Cl 1,2,4,5-tetraklórbenzol 1,2,4,5-Tetrachlorobenzene Cl Cl tri- ,terta-, penta-, hexaszubsztituált Cl Cl Cl Cl Cl Cl Cl 1,2,4-triklórbenzol 1,2,4-Trichlorobenzene Cl Cl Cl Cl Cl Cl 1,2,4,5-tetraklórbenzol 1,2,4,5-Tetrachlorobenzene Cl
pentaklórbenzol Pentachlorobenzene Cl Cl hexaklórbenzol Hexachlorobenzene aromás vegyületek tipikus és speciális reakciói: tipikus: szubsztitúció speciális: addíció Bruckner II/1 240 Cl + HCl Cl2 hν (UV) H kat. FeCl3 AlCl3 3 Cl2 Cl Cl H Cl H Cl H Cl H Cl H o-diklór benzol Cl Cl Cl Cl + perhalogénezés (csak sok Cl2 kell): minden lépésben: +Cl2 és -HCl Cl Cl Cl Cl Cl 1,2,4,5-tetraklór benzol Cl Cl Cl Cl p-diklórbenzol 1,2,4Cl triklórbenzol Cl Cl Cl Cl Cl Cl Cl Cl Cl Toluolszármazékok p -klórtoluol 4-klórtoluol 1-Chloro-4-methylbenzene CH3 CH3 Cl CH3 Cl Cl m-klórtoluol 3-klórtoluol Cl 2,4,6-triklórtoluol Cl 1-Chloro-3-methylbenzene 1,3,5-Trichloro-2-methylbenzene Kondenzált policiklusos szénhidrogénszármazékok Br Br CH3 Br 8 5 8 5 1 4 1-brómnaftalin 1-Bromonaphthalene 2-bróm-1-metilnaftalin 2-Bromo-1-methylnaphthalene 9 10 1 4 9-brómantracén 9-Bromoanthracene Szélső gyűrűkkel
kezdjük a számozást KÖZÉPEN, anellált C atomokat számozzuk utolsóként!! CCl3 Nev. gyak Cl 1 4 5 CH 1 DDT rovarirtószer (betiltották) Cl 1-Chloro-4-(5-chloro-1-trichloromethyl-pent-3-enyl)-benzene 1-klor-4-(5-klór-1-triklormetil-pent-3-enil)-benzol 1-bisz(4-klórfenil)-2,2,2-triklóretán DDT szintézise: (Zeidler, 1874) becenév: diklór-difenil-triklóretán H2SO4 -H2O 1962 klorálhidrát Bruckner II/1 271 klorál (triklór-acetaldehid) 1. rovarirtó-szer 2. lerakódik algákban kedvező hatás pusztítja a halakat 3. idegrendszeri károsodást okoz káros hatás (feszültségfüggő Na+-csatornák nyitva maradnak, depolarizáció, ezért az akciós potenciál kialakulása zavart lesz) X. Aromás hidroxivegyületek és származékai Egy vagy több hidrogént OH-ra cserélünk Az -OH helye szerint: -magban szubsztituált (fenol), -oldalláncban szubsztituált (aromás alkohol) Alapnevek: benzol fenol , naftalin naftol, fenantrén
fenantrol Szn: alapneveiből (pl. benzol, fenantrol) képezzük (pl jódfenol, 5-brómfenantrol) 1. Fenol típusú hidroxivegyületek: OH Egyértékű fenolok: OH OH OH CH3 CH3 fenol Phenol o-krezol o-cresol 2-Methyl-phenol m-krezol m-cresol 3-Methyl-phenol CH3 p -krezol p -cresol 4-Methyl-phenol kérdés: miért savanyúbb a fenolok kémhatása mint az alifás alkoholoké? pKa = 9.9 (fenol), 18 (ciklohexanol), 16 (etanol), 16 (víz), 48 (ecetsav) OH O + H 20 fenol H30 + fenolát anionok O O O válasz: A keletkező fenolát anion konjugáció révén stabilizálódik, az egyensúly ezért ennek javára eltolódik kérdés: hogyan befolyásolják a szubsztituensek a fenol kémhatását? memo: a p-krezolban a konjugáció kb. annyira kiterjedt mint a fenolban, de a p-nitrofenolban viszont kiterjedtebb, ami tovább növeli a savas karaktert. memo: az eltérő savasság eltérő vízoldhatóságot eredményez: pKa = 9.9 (fenol), 16 (víz), 18 (ciklohexanol) OH O +
NaOH erõsebb sav gyengén vízoldható H 20 a fenolok disszociációja vízben 10000-szerese a + HOH ciklohexanolénak töltött részecskék megjelenése megnövekedett oldhatóság gyeng bázis Na vízoldható OH O Na + NaOH gyengébb sav alig vízoldható H20 + H2O erõsebb bázis vízoldható OH OH OH kétértékű fenolok: három különböző izomer OH OH rezorcin Benzene-1,3-diol pirokatechin Benzene-1,2-diol háromértékű fenolok: három különböző izomer OH OH OH OH OH HO OH pirogallol Benzene-1,2,3-triol benzol-1,2,3-triol naftolok: OH oxihidrokinon Benzene-1,2,4-triol benzol-1,2,4-triol OH •redukáló-szer: AgNO3 – fotó előhívás •„depigmentáció” OH f loroglucin Benzene-1,3,5-triol benzol-1,3,5-triol OH OH 1-naftol (a-naf tol) 1-Naphthol antrolok: OH hidrokinon Benzene-1,4-diol 2-naf tol (-naftol) 2-Naphthol OH 1-antrol (a-antrol) 9-antrol (antranol) 1-Anthrol 9-Anthrol memo: rendhagyó nevezéktan
1-naftol és nem naft-1-ol 1-antrol és nem antr-1-ol fenantrolok: 2-fenantrol 2-Phenanthrol HO OH OH Nev. gyak OH OH Br CH3 CH3 OH Br H2C NO2 2,4-dibrómfenol 2,4-Dibromophenol 4-nitrofenol (p-nitrofenol) 2-Methylbenzene-1,3-diol 2-metilbenzol-1,3-diol CH3 4-etil-2-metilfenol 4-Ethyl-2-methylphenol 4-Nitrophenol Példa: OH 4-(2-Amino-1-hydroxyethyl)benzene-1,2-diol 4-(2-amino-1-hidroxietil)benzol-1,2-diol noradrenalin OH OH OH CH2 CH NH2 COOH OH OH 2-Amino-3-(3,4-dihydroxyphenyl)propionic acid 2-amino-3-(3,4-dihidroxifenil)propionsav CH 4-(2-Amino-1-hydroxyethyl)benzene-1,2-diol 4-(2-amino-1-hidroxietil)benzol-1,2-diol noradrenalin stressz hormon, OH CH2 NH2 neurotranszmitter, gyógyszerként: vérnyomás emelő OH OH DOPA 3,4-dihidroxyphenylalanine neurotranszmitter prekurzor: dopamin, + Parkinson-kór kezelése CH2 CHnoradrenalin NH2 2. Aromás alkoholok: CH2OH CH2OH OH CH2OH CH C fenilmetanol Phenylmethanol OH (2-Hydroxymethyl)phenol
trif enilmetanol (2-hidroxibenzil)-alkohol Triphenylmethanol szalicilalkohol, szaligenin benzil-alkohol benzylalcohol 3. Fenoléterek: OCH3 HC H 2C CH3 CH2OH 3-Phenyl-prop-2-en-1-ol 3-fenil-prop-2-én-1-ol fahéjalkohol 2-Phenylethan-1-ol 2-feniletan-1-ol fenetil-alkohol OCH3 CH H2C H2C O O H2C anizol metoxibenzol fenil-metil-éter Methoxybenzene CH2 etoxibenzol etil-fenil-éter Ethoxybenzene (alliloxi)benzol allil-fenil-éter (Allyloxy)benzene Fenoléterek előállítása: Savas jellegük miatt már NaOH-dal is fenolátot képeznek (Williamson szint.), míg az alkoholok csak fém Na-mal adnak alkoholátot! CH CH2 esztragol 1-allil-4-metoxibenzol 1-Allyl-4-methoxybenzene OH CH3 O Na OC2H5 NaOH C2H5-I -H2O -NaI H3C CH3 4. Kinonok: már nem aromás vegyületek +1 +2 +1 +2 memo: könnyen oxidálhatók a fenolok és redukálhatók a kinonok hidrokinon memo: A fekete-fehér fényképezés során a lemezre rétegelt AgBr szemcséket fénnyel
aktiváljuk. Előhíváskor a hidrokinon redukálja az Ag + fém Ag-é, ami fekete szemcseként rögzül a negatívon és ami a „negatív kép” sötét része. hidrokinon HO 1,4-benzokinon OH + AgBr* O O + 2Ag + 2HBr memo: neve kinon de nem kinoidális szerkezetű a molekula OH Példák: CH3 HO O O H C H kámforkinon flavanon [NÉT1 198] OH O O 1,7,7-Trimethylbicyclo[2.21]heptane-2,3-dione 1-Methylbicyclo[2.21]heptane-2,3-dione 5,7-Dihydroxy-2-(4-hydroxyphenyl)chroman-4-one kámforkinon - fogtömések egyik komponense O CH3 K2 vitamin CH3 CH2 CH O 2-Methyl-1,4-naphthoquinone C [Stryer 255] CH2 H 6 szükséges a protrombin és más kalciumkötő fehérjék szintézisénél (vérkoagulációs hatás), gyermekkorban: egészséges csontfejlődés O H3C plasztokinon A oxidált forma ( a redukáltf orma a hidrokinon) [NÉT1 57], Stryer 659 H3C O 2,3-Dimethyl-1,4-benzoquinone 9 fotoszintézis: fény hatására vízből O2-t fejlesztve redukálódik a
plasztokinon A A mitokondrium oxidáló szere: Koenzim Q és NADH az oxidációs rendszer nélkülözhetetlen részei O CH3O -2 CH3 +2 CH3O CONH2 N cukor R O + H+ NADH redukált Koenzim Q oxidált H H H CH3O OH -1 CH3 +1 CH3O R Koenzim Q redukált XI. Aromás kénvegyületek SH HS SH CH2 SH CH3 Benzenethiol benzoltiol tiofenol cukor OH R:= 10 izoprén egység (membránba horgonyzás) 1. Tiolok N Br 3-Methylbenzene-1-thiol Phenylmethanethiol 4-Bromobenzene-1-thiol fenilmetántiol 3-metilbenzol-1-tiol 4-bróm-benzol-1-tiol m-tiokrezol p-brómbenzol-1-tiol NAD+ oxidált CONH2 S S 2. Szulfidok CH3 difenil-szulfid diphenyl sulfide Methylsulfanylbenzene metil-fenil-szulfid methyl phenyl sulfide 3. Szulfoxidok 4. Szulfonok O O S S C3H7 O fenil-propil-szulfon phenyl propyl sulfone difenil-szulfoxid diphenyl sulfoxide 5. Szulfonsavak SO3H SO3H CH3 benzolszulfonsav Benzenesulfonic acid p-toluolszulfonsav Toluene-4-sulfonic acid 6.
Szulfonsav-észterek SO3H SO3CH3 4-aminobenzolszulfonsav 4-Aminobenzenesulfonic acid SO3H COOH Methyl benzenesulfonate metil-benzolszulfonát Benzenesulfonic acid methyl ester benzolszulfonsav-metil-észter 7. Szulfonsav-kloridok, szulfonsav-amidok 4-Sulfobenzoic acid 4-szulfobenzoesav p-szulfobenzoesav NH2 tozil-klorid p-toluolszulfonil-klorid 4-Methylbenzenesulfonyl chloride 4-metilbenzolszulfonil-klorid SO2Cl SO2NH2 SO2Cl CH3 benzolszulfonil-klorid Benzenesulfonyl chloride CH3 p-toluolszulfonamid Toluene-4-sulfonamide XII. Aromás nitrogéntartalmú vegyületek Előtag: nitro-, nitrozo- 1. Aromás niro- és nitrozovegyületek típusnév: nitro-arén, nitrozo-arén NO2 NO2 O2N nitrobenzol Nitrobenzene O2N 1,3-dinitrobenzol m-dinitrobenzol 1,3-Dinitrobenzene NO2 NO2 NO2 O2N 1,3,5-trinitrobenzol CH3 1,3,5-Trinitrobenzene 2,4,6-trinitrotoluol (TNT, trotil) 2,4,6-trinitrotoluene O2N NO NO2 NO2 CH2 1-nitronaftalin (a-nitronaftalin) 1-Nitronaphthalene
nitrozobenzol Nitrosobenzene fenilnitrometán Phenylnitromethane Néhány „robbanékony” nitrobenzol származék: OH O 2N NO2 ammónium-pikrát NO2 Trinitrotoluol (TNT) Pikrinsav (sói a pikrátok) kémcső kísérlet (max. 1g anyaggal) memo: fokozottan explozívak a TNT szubsztituált származékai pl.: trinitro metakrezol (ekrazit) pl. memo: tárolási, stabilitási okok miatt NH3 sói formában használjuk trinitrofluroglucin (TNFG) memo: hevesebb mint a TNT tetranitro-N-metilanilin (tetril) memo: még hevesebb gyutacsnak használták vas-pikrát (igen explozív) kémcsöves kísérlet TILOS! max. 1g anyag 2. kísérlet: süvítve kilő 1. kísérlet: gyűrtpapír! alufólia gyújtópálcával vagy gyufával a papírt meggyújtjuk Bunsen-égő 1. 2. TNT pikrinsav kormozó láng kilő TNFG heves, sistereg TILOS „tetril” még fényesebb TILOS fekete lőpor (Kina XI. század tűzijáték): helyes aránya a szénpor (tüzelőanyag) + kén
(tüzelőanyag) + salétrom (KNO3 oxidálószer) keverékének. Robbanásszerű térfogatnövekedés (pl. CO2) bizt a tolóerőt memo: Stroncium-nitrát segítségével vörösre, bárium-nitrát révén zöldre, réz-karbonáttal pedig kékre lehet változtatni a robbanás színét. füst nélküli lőpor: cellulóz nitrát szilárd hajtóanyag: Al és NH4ClO4 (ammónium-perklorát) (űrtechnika) gyufafej: KClO3 (kálium-klorát oxidálószer) + szénpor, kén és antimonszulfidok (Sb2S3 és Sb2S5 narancssárga) (tüzelőanyagok) keveréke. Égés során keletkező gázok: pl. CO2, SbO, SO2 memo: a gyufásdoboz dörzsfelületén vörös foszfort (P4) van, ami a súrlódás hatására könnyen meggyullad, azaz iniciátor. Robbanószerek jellemzése, az oxigénmérleg: kérdés: hány O2 molekula kell a szerves anyag elégetéséhez, ha azt feltételezzük, hogy CO2, N2, H2O keletkezik? 2 C3H5N3O9 – ½ O2 = 6 CO2↑ + 5 H2O↑ + 3 N2↑ CH2 O NO2 CH O NO2 CH2 O Alfred
Nobel egy mol. belül van mind a NO2 csop (oxidálószer) 1833-1896 mind a CH2 és CH (tüzelőanyag). Ezért igen hatékony! Összesen 14 mol gáz és gőz keletkezik: kvázi nullszaldós oxigénmérleg NO2 nitroglicerin (színtelen foly.) dinamit: diatomaföldbe (kovaföld, üledékes kőzet) felitatott nitroglicerin 2 C7H5N3O6 + 10,5 O2 = 14 CO2↑ + 5 H2O↑ + 3 N2↑ „TNT” 22 mol gáz és gőz keletkezik 2 C6H3N3O9 + 4,5 O2 = 12 CO2↑ + 3 H2O↑ + 3 N2↑ 18 mol gáz és gőz keletkezik „TNFG” 2. Aromás aminok és iminek típusnév: arilamin , arilimin H Ar Ar Ar N Ar H primer aromás amin (aril-amin) Ar N N H Ar szekunder aromás amin (diaril-amin) tercier aromás amin (triaril-amin) A. Egyértékű primer aminok NH2 NH2 NH2 NH2 H 3C CH3 anilin NH2 o-toluidin m-toluidin CH3 NH2 NH2 OH 2-aminof enol o-aminof enol 2-Aminophenol 1-naftil-amin (a-naftil-amin) 2-naftil-amin (-naftil-amin) p -toluidin B. Egyértékű szekunder
aminok H N H N bisz(2-naftil)-amin Bis(2-naphthyl)amine difenil-amin Diphenylamine H3C C. Egyértékű tercier aminok C6H5 C6H5 CH3 N N C6H5 trifenil-amin N ,N-dimetilanilin N ,N-Dimethylaniline Triphenylamine D. Kvaterner ammóniumvegyületek CH3 H3C OH N H3C CH2 Cl H3N benzil-trimetil-ammónium-hidroxid Benzyltrimethylammonium hydroxide anilinium-klorid anilinium chloride E. Többértékű aminok naf talin-1,4-diamin Naphthalene-1,4-diamine NH2 NH2 NH2 NH2 p -fenilén-diamin p -Phenylenediamine Benzene-1,4-diamine NH2 NH2 bifenil-4,4'-diamin Biphenyl-4,4'-diamine F. Aromás iminek CH3 HC HN CH N benzilidénimin Benzylideneimine N-etilidénanilin N-Ethylideneaniline 3. Aromás hidroxilamin és hidrazinszármazékok típusnév: aril-hidroxilamin Utótag: hidroxilamin Előtag: hidroxilamino HO NH HO C2H5O NH NH OH N -fenilhidroxilamin 4-(hidroxiamino)fenol N-Phenylhydroxylamine 4-(Hydroxyamino)phenol O-Ethyl-N-phenylhydroxylamine
O-etil-N-f enilhidroxilamin Utótag: hidrazin Előtag: hidrazino típusnév: aril-hidrazin CH3 HN NH2 fenilhidrazin Phenylhydrazine NH2 HN NH HN N-metil-N ,-fenilhidrazin OH 4-hidrazinofenol N-Methyl-N'-phenylhydrazine 4-Hydrazinophenol 4. Aromás azo- és azoxivegyületek típusnév: azoarén Előtag: azo Utótag: diazén N Szimmetrikus aromás azovegyület N difenildiazén Diphenyldiazene azobenzol azobenzene Aszimmetrikus aromás azovegyület N 4 1 H2N CH3 N C6H5 N 4-(fenilazo)toluol 4-(phenylazo)toluene Phenyl-p-tolyldiazene fenil-p-tolildiazén N 1 C6H5 N N 4 1 N C6H5 N 4-(fenilazo)benzol-1,3-diamin 4-(Phenylazo)benzene-1,3-diamine N (krizoidin)N NH2 NH2 NH2 1-(fenilazo)naftalin-2-amin 1-(Phenylazo)naphthyl-2-amine NH2 4-(fenilazo)naftalin-1-amin 1-(fenilazo)naftalin-2-amin 4-(Phenylazo)naphthyl-1-amine 1-(Phenylazo)naphthyl-2-amine C6H5 N N 4 1 NH2 4-(fenilazo)naftalin-1-amin 4-(Phenylazo)naphthyl-1-amine kérdés: mi lehet a szín
molekuláris oka? válasz: a megfelelő kromofor csoport nyeli el a fényt - a finomhangolást a konjugáció kiterjedésének mértéke biztosítja memo: chroma = szín, phoros = hordozó (görög) itt: konjugált kettős-kötés rendszer sárga 4-nitroazobenzol N elnyelés: 420-430nm O N N kérdés: miért lehet színes egy azovegyület? memo: a fehér fény (400-800 nm) 2 1. – teljes spektrumból szelektíven nyel el egy tartományt 2. – a megmaradó komponensek O2N keverék színét érzékeljük sárgásvörös 4-nitro-4’-aminoazobenzol NH2 N N CH3 N N O2 N N CH3 sötétvörös 4-nitro-4’-(N,N-dimetilamino)azobenzol elnyelés: 500-520nm memo: más kromofórok is finomhangolhatók pl. konjugált ketonok Otto Nikolaus Witt 1853-1915 H3C aceton színtelen C O O H 3C CH3 C H 3C O C O biacetil H3C sárga C CH3 C C O O 2,3,4-triketopentán narancssárga Példa: HO H2N NH2 4 H2N NH2 2 N N N N N N HO HO3S 1,3- bisz[ (2,4-d iaminof enil)
azo ]-be nzol (Bismarc k-b arn a) SO3H N N HO3S 4-(2-hidro benzolszul 4-(2-Hydro ben (-naftolo 4-(2-hidroxinaftalin-1-ilazo)benzolszulfonsav 4-(2-Hydroxynaphthalen-1-ylazo)benzenesulfonic acid (-naftoloranzs 450-510nm) N N NH2 NH2 N N 4,4,-bisz(1-amino-4-szulfonaftalin-2-ilazo)bifenil (kongóvörös: legerõsebb sáv 400-560nm között) SO3H Congo Red: a strong absorption band at 340nm (near-UV) and another at 500nm (at blue-green transition region). This dye transmits red wavelengths above 560 nm and thus, appears red to the eye. azoxivegyületek COOH O N N N N O N,N '-Diphenyldiazene N -oxide N,N'-difenildiazin-N -oxid azoxibenzol 2-(Phenyl-O,N,N-azoxy)naphthalene-1-carboxylic acid 2-(fenil-O,N,N -azoxi)-1-naftalin-1-karbonsav 5. Aromás diazónium vegyületek típusnév: aréndiazonium N2 N2 Cl Előtag: diazónio Utótag: diazónium OH N2 8 1 BF4 SO3 benzoldiazonium-klorid Benzenediazonium chloride 8-hidroxinaftalin-1-diazonium
tetrafluoroborát 4-diazoniobenzol-1-szulfonát 4-Diazoniobenzene-1-sulfonate 8-Hydroxynaphthalene-1-diazonium tetraf luoroborate A diazónium kation fontos poláris határszerkezetei: N N N N N N N N N N Bruckner II/1 565 A benzoldiazónium-klorid előállításának részletei: Itt nincs meg az elektron-oktett!: potens elektrofil a bruttó reakció: néhány részlet: N-nitrozo-ammónium kation arilamin H N H H N O -H+ N N O H N N OH -H2O +H Bruckner II/1 569 N N Diazónium kation Diazohidroxid H N N O N-nitrozoamin Aromás diazónium vegyületek tipikus reakciói: gyökös Sandmeyerszerű reakciók: „azokapcsolás” : Cl OH N N H Cu2O, Cu2+, H2O Ar Cl OH SE OH CuX X=Cl, Br, CN N2 Ar Cl X N N KI Ar N3 I H N3 -HX HBF4 + hõ Ar OH F N H3PO2 + H2O N Ar H 6. Aromás azidovegyületek típusnév: azidoarén és aril-azid Szn Csn N3 Előtag: azido Utótag: nincs Az azidobenzol két poláris
határszerkezete: N3 SO3H instabil robbanékony f enil-azid Azidobenzene azidobenzol 1-azidonaftalin-2-szu f enil-azid azobenzol származékok (szinezékek) 1-Azidonaphthalene-2 Azidobenzene azidobenzol elektrofil szubsztitúció 1-azidonaftalin-2-szulfonsav 1-Azidonaphthalene-2-sulfonic acid N N N N N N XIII. Aromás oxovegyületek 1. Aromás aldehidek - típusnév: arilaldehid Képzés: az arilkarbonsav nevének megfelelő csonkított acilnévből az pl.: ftáloil ftálaldehid, naftoil naftaldehid Triviális savnév esetén csonkított acilnév + aldehid pl.: benzoil +aldehid benzaldehid A gyűrűhöz közvetlenül csatlakozó aldehideket karbaldehideknek hívjuk pl.: naftalinkarbaldehid aldehid utótaggal képezzük A) Karbaldehidek CHO CHO CHO OH OH 2-hidroxibenzaldehid 2-Hydroxybenzaldehyde 3-hidroxibenzaldehid 3-Hydroxybenzaldehyde CH3 4-metilbenzaldehid 4-Methylbenzaldehyde Előtag: formil Utótag :karbaldehid Példa: CHO CHO 2 CHO HC
CH 3 OCH3 OH 4-hidroxi-3-metoxibenzaldehid vanillin OCH3 3-fenilakrilaldehid fahéjaldehid 4-Hydroxy-3-methoxybenzaldehyde 3-Phenylprop-2-enal B) Alifás oldalláncú aromásaldehidek CHO CHO CH H2C CHO [(1-naftil)metil]-malonaldehid H2C (1-naftil)acetaldehid 4-metoxibenzaldehid ánizsaldehid 4-Methoxybenzaldehyde 2. Aromás ketonok Szn.: előtag: oxo típusnév: alkanon utótag: on Csn.: keton C O A) az alifás oldallánc része az O karbonilcsoport oxocsoport H3C H3C C O O O CH2 CH3 CH O2 CH2 CH2 CH3 O C CH3 CH O2 CH2 C CH3 O 1-Phenylbutan-2-one O 1-Phenylpropan-2-one 1-Phenylethan-1-one 1-fenilpropán-2-on 1-fenilbután-2-on 1-feniletan-1-on 1-f enilbutan-2-on f enilaceton acetof enon 1-Phenylbutan-2-one 1-Phenylpropan-2-one 1-Phenylethan-1-one fenil-metil-keton benzil-etil-keton benzil-metil-keton 1-fenilpropán-2-on 1-fenilbután-2-on 1-feniletan-1-on methyl-phenyl keton 1-f enilbutan-2-on f enilaceton acetof enon B) Az karbonilcsoport két
aromás gyűrűhöz benzil-etil-keton kapcsolódik fenil-metil-keton benzil-metil-keton O methyl-phenyl keton O Szn. Csn. C Csn. fenil-(2-naftil)-keton Szn. Naphthalen-2-yl-phenyl-methanone C benzofenon difenil-keton difenilmetanon Diphenylmethanone C) Aromás di-, tri- és poliketonok O C D) Aromás rendszerekhez integrálódott ketonok O O C C O C inden-1-on C C Inden-1-one O O dif enil-diketon 1,2-Diphenylethane-1,2-dione 1,2-difeniletán-1,2-dion f luorén-9-on bisz(2-naf til)-diketon O Di(2-naphthyl)ethane-1,2-dione C di(2-naftil)etán-1,2-dion CH2 Fluoren-9-one O O C C 1,2-dihidronaftalin-1-on 9 10 1,2,-Dihydronaphthalen-1-one CH2 C O Csn. bisz(2-naf til)-diketon Di(2-naphthyl)ethane-1,2-dione Szn. di(2-naftil)etán-1,2-dion memo: H2 C 1 2 CH2 1,2-Dihydronaphthalene 1,2-dihidronaftalin antron 9,10-dihydroanthracen-9-one 9,10-dihidroantracén-9-on XIV. Aromás karbonsavak: Az aszpirin rövid története - A fűzfakérget az ókori
Ázsiában is használják (2400 éve) láz és fájdalomcsillapításra, - 1830-tól a fűzfakéreg extraktumát használják hasonló célból, - 1840 körül azonosítják a kivonat aktív komponensét a szalicint (salix [latin] fűzfa) - 1870 Nencki (Bázel) kimutatja hogy a szervezetben szalicilsavvá alakul át a szalicin (a szalicilsav is fájdalom és lázcsillapító, de égeti a nyelőcsövet, gyomrot) - 1875 Patikusok elkészítik a Na+ sóját, „működik”, de borzasztó az íze, hánytat - 1890 Félix Hofmann/Arthur Eichengrün(??) (Bayer) elkészíti az aszpirint, ami jól hat és elfogadható ízű: „a” acetilt, „spir” spirea-t (gyöngyvessző melyből szalicilsav-metilészter izolálható) - 1898 Az aszpirin klinikai kipróbálása és üzemi gyártása (Bayer) - 1990 Csak az USA-ban > 10 millió kg-t gyártanak évente Hatásmechanizmus: az aspirin, mint acetilezőszer a ciklooxigenáz (COX) inhibitora, gátolja a szintézist) prosztaglandin -
gyulladáscsökkentő, - a köszvény és reuma hatásos gyógyszere Ciklooxigenáz-arahidonsav komplex Loll, P.J, Picot, D, Garavito, RM (1995) NatStructBiol 2: 637-643 Harman, C.A, Rieke, CJ, Garavito, RM, Smith, WL (2004) JBiolChem 279: 42929-42935 H2N Ser H2N O Ser-Ac O O CH2 OH CH3 CH2 Szerin TreoninC OH H2N O CH C OH SH O C O O O C 2N CCH OH OH H2N HCH C HCH CH C OH H2N CH 2N OH CH2 CH2 CH C OH H2N C OH C CH OH2 C O CiszteinSzerin NH CH2 3 C N O H2N T Szintézis tervezet: a fenolból aszpirin Bruckner: II/703 II/726 II/860 kőszén, petróleum memo: gyomorban nem, bélben hidrolizál (ecetsav + szalicilsav) Kolbe-szintézis: / 100 atm memo: az aszpirin gátolja a ciklooxigenázt, amely prosztaglandin szint. része, így ennek csökkenése a fájdalomküszöböt növeli és a gyulladást csökkenti. XIV. Aromás karbonsavak Az aromás gyűrűhöz kapcsolódó vagy annak oldalláncában a láncvégi metilcsoport hidrogénjeit
cseréljük: 2 db H-t O-ra; 1 db H-t OH-ra karboxilcsoport kapcsolódása szerint: arénkarbonsav arilezett alifás karbonsav karboxilcsoportok száma szerint: egy-, két-, három- és több-bázisú sav szénhidrogén oldallánc: telített telítetlen Előtag: karboxi Utótag :karbonsav Nostradamus (1556) 1. Arénkarbonsavak típusnév: arénkarbonsav COOH A. Egyértékű savak: tartósítószer (gombák, baktériumok benzolkarbonsav szaporodását gátolja): benzoesav E210, E211, E212, E213 Benzoic acid COOH 1 2-naf toesav 2-naphtoic acid COOH COOH COOH COOH CH3 2 3 H3C 2-metilbenzoesav o-toluilsav 3-metilbenzoesav m-toluilsav 2-Methylbenzoic acid 3-Methylbenzoic acid 1 4 COOH 2-naf toesav CH3 2-naphtoic acid 4-metilbenzesav p-toluilsav 4-Methylbenzoic acid 1 1-naf toesav 1-naphtoic acid B. Kétértékű savak: COOH COOH COOH HOOC 1 4 1 2 3 COOH COOH COOH COOH COOH 1,4-benzoldikarbonsav benzene-1,4-dicarboxylic acid o tereftálsav
COOH HOOC op=425 COOH Terephthalic acid grafit szerkezetigazoló benzol-1,2.3-trikar benzol-1,3,5-trikarbonsav oxidációja (hemimellitsav) kérdés: miért ennyire eltérő a három szerkezeti izomer(trimezinsav) olvadáspontja? Benzene-1,3,5-tricarboxylic acid Benzene-1,2,3-tric benzol-1,2-dikarbonsav benzene-1,2-dicarboxylic acid op=231o ftálsav Phthalic acid benzol-1,3-dikarbonsav benzene-1,3-dicarboxylic acid op=348o izof tálsav Isophthalic acid memo: intermolekuláris H-hidak Bruckner II/1 799 COOH C. Többértékű savak: COOH COOH HOOC COOH HOOC COOH COOH HOOC COOH COOH benzol-1,2.3-trikarbonsav benzol-1,3,5-trikarbonsav (hemimellitsav) (trimezinsav) Benzene-1,3,5-tricarboxylic acid Benzene-1,2,3-tricarboxylic acid COOH benzol-1,2,3,4,5,6-hexakarbonsav (mellitsav) Benzene-1,2,3,4,5,6-hexacarboxylic acid O D. peroxisavak: O O C H C O perbenzoesav peroxibenzoesav perbenzoic acid O O H O H C diperoxi-ftálsav O O rossz a benzolperoxikarbonsav
mert rossz a benzol-1,2-diperoxikarbonsav a benzolkarbonsav név sem használható a benzoesav helyett mert af tálsav helyett nem mondhstjuk hogy benzol-1,2-karbonsav 2. Arilezett alifás karbonsavak Előtag: karboxi típusnév: arilalkánsav A. Telített oldalláncú: Utótag :sav H3C 2 COOH CH 3 CH2 COOH CH2 CH2 COOH f enilecetsav Phenylacetic acid 3-fenilpropánsav hidrof ahéjsav 2-fenilpropánsav hidratropasav 3-Phenyl-propanoic acid 2-Phenyl-propanoic acid konstitúciós izomerek B. Telítetlen oldalláncú: H2C COOH C 2-fenilakrilsav (atropasav) H H C C 2-Phenylacrylic acid C C H nev. gyak H2 H2 H3C 5 C 3 C CH CH COOH 1 H COOH cisz-3-fenilpropénsav (allofahéjsav) transz-3-fenil-propénsav (f ahéjsav) 3-Phenylacrylic acid 3-Phenylacrylic acid CH3 sztereo izomerek HOOC CH2 3-metil-5-(1-naftil)hexánsav 3-Methyl-5-(1-naphthyl)hexanoic acid 5 1 HOOC COOH H2 C 3 C H2 COOH 3-(2-karboxietil)-5-(karboximetil)benzoesav
3-(2-Carboxyethyl)-5-(carboxymethyl)benzoic acid 3. Magban szubsztituált arénkarbonsavak Előtag: karboxi COOH Utótag :karbonsav típusnév: arilkarbonsav COOH COOH COOH COOH Cl 1 O2N Cl H 2N NO2 1 COOH 1 1 NH2 2-klórbenzoesav o-klórbenzoesav 2-Chlorobenzoic acid 2-aminobenzoesav 4-aminobenzoesav p-aminobenzoesav o-aminobenzoesav 2-nitrobenzoesav 1-klórnaftalin-2-karbonsav (antranilsav) o-nitrobenzoesav 1-Chloronaphthalene2-Aminobenzoic acid 4-Aminobenzoic acid 2-Nitrobenzoic acid 2-carboxylic acid H 2N COO NO2 2,4,6-trinitrobenzoesav 2,4,6-Trinitrobenzoic acid COOH IkerionosCOOH szerkezet: COOH NO2 protonCOOH O2N H 2N COOH NO2 H 3N 4 2 NH2 NH2 2-aminobenzoesav o-aminobenzoesav (antranilsav) 2-Aminobenzoic acid 4-aminobenzoesav p-aminobenzoesav 4-Aminobenzoic acid NO2 2-aminobenzoesav o-aminobenzoesav 2,4,6-trinitrobenzoesav (antranilsav) 2,4,6-Trinitrobenzoic acid acid 2-Aminobenzoic =7.58 Debye 4-aminobenzoesav p-aminobenzoesav
4-Aminobenzoic acid COOH COOH COOH COOH OH HO OCH3 OH 2-hidroxibenzoesav o-hidroxibenzoesav (szalicilsav) OH 3,4,5-trihidroxibenzoesav (galluszsav) 2-Hydroxybenzoic acid 3,4,5-Trihydroxybenzoic acid OH 4-hidroxi-3-metoxibenzoesav (vanillinsav) 4-Hydroxy-3-methoxybenzoic acid OCH3 4-metoxibenzoesav p-metoxibenzoesav (ánizssav) 4-Methoxybenzoic acid 4. Arilezett alifás karbonsavak szubsztituált származékai COOH típusnév: aralkilsav (pl. akrilsav szárm : CH2=CHCOOH) Előtag: karboxi COOH COOH Utótag :karbonsav C H H H C C H H OCH3 C C HOOC OH H OCH3 C OH OH 3,4-dimetoxibenzoesav (verátrumsav) 3,4-Dimethoxybenzoic acid OH 3-(2,4-dihidroxifenil)akrilsav 3-(2-hidroxifenil)akrilsav (kávésav) transz (o-kumársav) transz 3-(2-hidroxifenil)akrilsav (o-kumarinsav) cisz 3-(2,4-Dihydroxyphenyl)acrylic acid 3-(2-Hydroxyphenyl)acrylic acid 3-(2-Hydroxyphenyl)acrylic acid nev. gyak O C 3 CH2 3 COOH 2-amino-3-(4-hidroxif enil)propánsav
(4-hidroxif enil)-alanin vagy tirozin C H NH2 2-Amino-3-(4-hydroxyphenyl)propanoic acid CH2 COOH 4-oxo-4-fenilbutánsav CH2 4-Oxo-4-phenylbutanoic acid OH 3-benzoil-propionsav O C O H2C C 5 3 H C COOH 3,5-dioxo-2-fenilvaleriánsav H 3,5-dioxo-2-f enilpentánsav 3,5-Dioxo-2-phenylpentanoic acid O O 5. Aromáskarbonsavak funkcionális származékai O C O O O O CH3 benzoesav-anhidrid O C O H2 O O O O A. Karbonsavanhidridek: O O benzoesav-anhidrid C benzoe CH C ftálsav-anhid H2 1,3-dihidrobe (ftálsavból hevítésre k Cbenzoesav-propionsav-an O ftálsav-anhidrid 1,3-dihidrobenzof urán-1,3-dion benzoesav-propionsav-anhidridO C (ftálsavból hevítésre könnyen képzõdik) B. Karbonsavészterek:O (o-dikarbonsav) O ftálsav-anhidrid O O CH3 C O C CH2 1,3-dihidrobenzof urán-1,3-dion dimetil-ftalát C CH3 O dimethyl phtalate O képzõdik) Bruckner II/ 1 825 C (ftálsavból hevítésre könnyen Ethyl benzoate Phthalic acid dimethyl ester etil-benzoát
O O C CH3 Benzoic acid ethyl ester benzoesav-etil-észter O benzoesav-anhidrid Csn COOCH3 O C O CH2 antracén-9-karbonsav-metil-észter Anthracene-9-carboxylic acid methyl ester ftalid 3H-Isobenzofuran-1-one COCl C. Karbonsavhalogenidek: COCl COCl OH szalicilsav-klorid COCl COCl (2-Hydroxybenzoyl) chloride (2-hidroxibenzoil)-klorid OCH3 benzoil-klorid Benzoyl chloride ftaloil-diklorid (4-Methoxy)benzoyl chloride (4-metoxi)benzoil-klorid Phthaloyl dichloride ánizssav-klorid CH3 D. Karbonsavamidok: CONH2 C NH O Phtalamic acid CONH2 CONH2 acetanilid COOH N-Phenylacetamide CONH2 benzoesav-amid benzamid tereftálsav-amid tereftálamid ftálamidsav Benzamide Terephthalamide Phthalamic acid O C O NH C ftálimid CH3 O Isoindole-1,3-dione NH C N-metilbenzamid N -Methylbenzamide E. Karbonsavnitrilek: CN CN CN benzonitril Benzonitrile benzoesavnitril ftalonitril Phthalonitrile ftálsav-dinitril NC fenil-izocianid Isocyanobenzene memo: ez nem nitril
hanem izocianid
gyűrűs molekula. Minden C-atomja sp2-es hibridállapotú. A 6 db pz atom-pályából, 3 db p molekula pálya alakul ki: aromás elektronszerkezetű vegyület. „szokatlan” hogy nem mutatják a alkének tipikus addíciós reakciói Addició (cisz) H H OH KMnO4 / H2O KMnO4 / H2O H H Addició (transz) semmi OH H H Br Br2 / CCl4 Br2 / CCl4 H Br H Br Subsztitúció H Br Br2 / FeBr3 + HBr CCl4 Br H semmi „szokatlan” stabilitása: A jósolt -28.6 kcal/mol, vagy ennek többszöröse DH-hoz képest, a mért hidrogénezési „hő” jelentős stabilitásra utal: a rezonancia energia jelentős (-36 kcal/mol). A benzol tehát ugyancsak inert! + 3 H2 kat. / nyomás DH = -49.8(kcal/mol) H 3*ciklohexén = -85.8 rezonancia stab. = +360 D H (kcal/mol) 85.8 -36.0 57.2 -1.8 -57.4 28.6 -55.4 -49.8 -28.6 H 0.0 Wade 693 aromás rendszerek (szakkifejezéssé alakult): •delokalizált p-rendszer (alternáló egyes és kettős kötések): 4n+2 p-elektron
részvételével (4-el nem osztható; azok: antiaromás / nem-aromás) •síkalkat •gyűrűs VIII. Aromás szénhidrogének Homoaromás vegyületek: benzol, benzolrészekből felépülő molekulák és azok származékai, amelyek lehetnek monociklusos, policiklusos és kondenzált ciklusos szénhidrogének. Heteroaromás vegyületek:aromás elektronszerkezet S, N, és O atomokkal. 1. Monociklusos aromás szénhidrogének Két szubsztituens relatív helyzete: orto (1,2), meta (1,3) és para (1,4) Három szubsztituens relatív helyzete: vicinális (1,2,3), aszimmetrikus (1,2,4), és szimmetrikus (1,3,5) A. Telített oldalláncú monociklusos aromás szénhidrogének Típusnevek: Toluene toluol (metilbenzol) Benzene benzol E(RHF/6-311++Gd,p) CH3 CH3 karcinogén!!! piros kék -0.03 töltés 003 CH3 •xylos (görög): fa •petrolkémia CH3 CH3 = 0 Debye p-elektronszextett 1,2-dimetilbenzol (orto-xilol) o-Xylene CH3 1,3-dimetilbenzol (meta-xilol) m-Xylene CH3
1,4-dimetilbenzol (para-xilol) p-Xylene CH3 H3C CH3 H C CH3 CH H3C H3C CH3 mezitilén 1,3,5-trimetilbenzol mesitylene kumol izopropilbenzol Isopropylbenzene CH3 para-cimol 1-metil-4-izopropilbenzol p-Cymene Csoportnevek: H3C phenyl fenil- H 3C H3C o-tolyl o-tolil- p -tolyl p-tolil- m-tolyl m-tolil- CH3 nev. gyak H3C benzil- H3C H 2C 1 C H2 C C CH3 H2 21 4 H3C CH2 1-(1,1-Dimethylbutyl)-4-ethyl-2-methylbenzene 1-(1,1-dimetilbutil)-4-etil-2-metilbenzol Faj: ILLATOS AROMÁS VEGYÜLETEK Név: Vegyület: Mandula (Prunus amygdalus) keserűmandula benzaldehid Kömény (Cuminum cyminum) köményolaj o-, m- és p- cimol Kömény (Cuminum cyminum) köményolaj chuminaldehid (illatos folyadék) Fahéj (Cinnamomum zeylanicum) fahéjaldehid fahéjaldehid benzoefa gyantája (Styrax benzoin) benzoegyanta trópusi fa XVI. sz óta ismert tolulbalzsam benzoesav toluol kérdés: helyettesíthetünk-e egy aromás hidrogént egy alkil csoporttal?
válasz: igen, Friedel–Crafts-alkilezési (SE2) reakció során megvalosítás: pl. alkil-halogenid + Lewis-sav H CH3 AlCl3 CH Cl + HCl + CH3 2-klórpropán kumol izopropilbenzol általánosítás: más potenciális karbokationt eredményező reagens is alkalmas, pl. propén, ciklohexén Solomons 670, Bruckner II-125 kumol cikklohexilbenzol B. Telítetlen oldalláncú monociklusos aromás szénhidrogének helyzetizoméria H2C CH3 HC HC vinilbenzol sztirol vinylbenzene styrole H2C CH2 CH propenilbenzol propenylbenzene HC HC e (f Eth CH CH2 CH2 allilbenzol H2C allylbenzene HC 1,4-divinilbenzol p -divinilbenzol 1,4-Divinylbenzene CH C CH etinilbenzol (fenilacetilén) kat. Solomons 693 >10 milliárd kg/év 2. Izolált policiklusos aromás szénhidrogének Biphenyl bifenil H2C diphenylmethane difenilmetán memo: a két aromás gyűrű se nem koplanáris se nem merőleges (~40o) tetr tetr = 0 Debye C piros kék -0.033 töltés
0033 methane tán tetraphenylmethane tetrafenilmetán Csoportnevek: transz – op: 125C C sztilbén 1,2-diphenylethene C CH 1,2-dif eniletén CH tolán diphenylacetylene C CH sztilbén difenilacetilén 1,2-diphenylethene C CH 1,2-dif eniletén tolán diphenylacetylene difenilacetilén C cisz – op: 5-6C tritil- 3. Kondenzált policiklusos szénhidrogének feltétel: legalább két közös szénatom: - lineáris anelláció - anguláris anelláció memo: a naftalin kivételével mindegyik név „én” végződésű kétgyűrűs rendszerek: naftalin (szintelen) folytonosan konjugált (6+4 π-elektr.) aromás (=0D, 6- és 6-tagú gyűrűk) molyirtó naftalin (szintelen) Bruckner II 185 azonos azulén (mélykék határszerkezetek krist.) magnólia Bruckner II 1377 folytonosan konjugált (6+4 π-elektron = 4*2+2 ← aromás) szemiaromás (=1.1D, töltés szepar,7- és 5-tagú gyűrűk) azulén (mélykék krist.) nem-azonos határszerkezetek
nem-aromás rendszer Bruckner II 193 (6+2 π-elektr.) ( dipol, 6- és 5-tagú gyűrűk) memo: az aromás gyűrűhöz kondenzált ciklopentadién fokozott reaktivitású C H H 1H-Indene indén (szintelen folyad.) fokozott reaktivitású („savanyú”) metilén csop. (pl - indén + Na - indén + aldehid) C H Na 10 p-elektron = 4*2 + 2 ← aromás három gyűrűs rendszerek: 12 p-elektron ← nem-aromás bifenilén Biphenylene antracén Anthracene H2C fenantrén fluorén Phenanthrene 2-Methyl-3-vinyl-1H-indene kékesen fluoreszkáló szintelen tûkristály fokozott reaktivitású („savanyú”) C metilén csoport (pl. – fluorén + Na) H Na memo: a kialakuló anion esetében az aromacitás ki tud terjedni a mol. egészére 14 p-elektron = 4*3 + 2 ← aromás memo: A naftalin rezonancia energiája (-60 kcal/mol) kicsit alacsonyabb mint a benzol kétszerese (-36kcal/mol*2= -72kcal/mol). Az antracéné -84kcal/mol, míg a fenantréné -91 kcal/mol (-108 helyett).
négy és több gyűrűs rendszerek: naftacén krizén Naphthacene Chrysene naftacén krizén Naphthacene Chrysene perilén pirén Perylene Pyrene memo: megtalálhatók a dohányfüstben, a diesel autók fekete füstjében, perilén pirén Perylene Pyrene pentacén Pentacene koronén Coronene Példa: (a máj méregtelenítési stratégiája, reaktív intermedier, majd a vízoldhatóvá tétel glutationnal) e d c b f aril hidroxiláz (májban) O benzo[def ]krizén Benzo[def ]chrysene ez a ténylegesen karcinogén hatású vegyület Az teljes SCF elektronsűrűség alapján számított izo-felületek 0.004 0.02 perilén bronzsárga krist. (op 274oC) memo: 2 naftalin peri helyzetű összekapcsolódása 0.004 0.025 0.04 0.04 koronén sárga, krist. (op 429oC) hat benzolgyűrű körkörös anellációja, ciklikusan kondenzált gyűrűs aromás szénhidrogén aromaticitás – nem összefüggő p rendszerek IX. Aromás halogénezett szénhidrogének Egy
vagy több hidrogént X-re cserélünk halogénezés helye szerint:-magban szubsztituált (aril-halogenid), -oldalláncban szubsztituált (aral-kilhalogenid) Szn: előző fejezet alapneveiből (pl. benzol, fenantrén) képezzük (pl. jódbenzol, 9-brómfenantrén) Csn: előző fejezet csoportneveihez (pl. fenil, fenantril) tesszük a funkció nevet (pl klorid) és így kapjuk a (pl. fenil-jodid, fenantril-bromid) Cl diszubsztituált Cl monoszubsztituált Cl Cl Cl klórbenzol chlorobenzene Cl 1,2-diklórbenzol (o-diklórbenzol) 1,2-Dichlorobenzene Cl 1,3-diklórbenzol Cl Cl Cl (m-diklórbenzol Cl 1,3-Dichlorobenzene 1,4-diklórbenzol 1,2,4-triklórbenzol Cl (p -diklórbenzol) Cl 1,2,4-Trichlorobenzene 1,4-Dichlorobenzene Cl 1,2,4,5-tetraklórbenzol 1,2,4,5-Tetrachlorobenzene Cl Cl tri- ,terta-, penta-, hexaszubsztituált Cl Cl Cl Cl Cl Cl Cl 1,2,4-triklórbenzol 1,2,4-Trichlorobenzene Cl Cl Cl Cl Cl Cl 1,2,4,5-tetraklórbenzol 1,2,4,5-Tetrachlorobenzene Cl
pentaklórbenzol Pentachlorobenzene Cl Cl hexaklórbenzol Hexachlorobenzene aromás vegyületek tipikus és speciális reakciói: tipikus: szubsztitúció speciális: addíció Bruckner II/1 240 Cl + HCl Cl2 hν (UV) H kat. FeCl3 AlCl3 3 Cl2 Cl Cl H Cl H Cl H Cl H Cl H o-diklór benzol Cl Cl Cl Cl + perhalogénezés (csak sok Cl2 kell): minden lépésben: +Cl2 és -HCl Cl Cl Cl Cl Cl 1,2,4,5-tetraklór benzol Cl Cl Cl Cl p-diklórbenzol 1,2,4Cl triklórbenzol Cl Cl Cl Cl Cl Cl Cl Cl Cl Toluolszármazékok p -klórtoluol 4-klórtoluol 1-Chloro-4-methylbenzene CH3 CH3 Cl CH3 Cl Cl m-klórtoluol 3-klórtoluol Cl 2,4,6-triklórtoluol Cl 1-Chloro-3-methylbenzene 1,3,5-Trichloro-2-methylbenzene Kondenzált policiklusos szénhidrogénszármazékok Br Br CH3 Br 8 5 8 5 1 4 1-brómnaftalin 1-Bromonaphthalene 2-bróm-1-metilnaftalin 2-Bromo-1-methylnaphthalene 9 10 1 4 9-brómantracén 9-Bromoanthracene Szélső gyűrűkkel
kezdjük a számozást KÖZÉPEN, anellált C atomokat számozzuk utolsóként!! CCl3 Nev. gyak Cl 1 4 5 CH 1 DDT rovarirtószer (betiltották) Cl 1-Chloro-4-(5-chloro-1-trichloromethyl-pent-3-enyl)-benzene 1-klor-4-(5-klór-1-triklormetil-pent-3-enil)-benzol 1-bisz(4-klórfenil)-2,2,2-triklóretán DDT szintézise: (Zeidler, 1874) becenév: diklór-difenil-triklóretán H2SO4 -H2O 1962 klorálhidrát Bruckner II/1 271 klorál (triklór-acetaldehid) 1. rovarirtó-szer 2. lerakódik algákban kedvező hatás pusztítja a halakat 3. idegrendszeri károsodást okoz káros hatás (feszültségfüggő Na+-csatornák nyitva maradnak, depolarizáció, ezért az akciós potenciál kialakulása zavart lesz) X. Aromás hidroxivegyületek és származékai Egy vagy több hidrogént OH-ra cserélünk Az -OH helye szerint: -magban szubsztituált (fenol), -oldalláncban szubsztituált (aromás alkohol) Alapnevek: benzol fenol , naftalin naftol, fenantrén
fenantrol Szn: alapneveiből (pl. benzol, fenantrol) képezzük (pl jódfenol, 5-brómfenantrol) 1. Fenol típusú hidroxivegyületek: OH Egyértékű fenolok: OH OH OH CH3 CH3 fenol Phenol o-krezol o-cresol 2-Methyl-phenol m-krezol m-cresol 3-Methyl-phenol CH3 p -krezol p -cresol 4-Methyl-phenol kérdés: miért savanyúbb a fenolok kémhatása mint az alifás alkoholoké? pKa = 9.9 (fenol), 18 (ciklohexanol), 16 (etanol), 16 (víz), 48 (ecetsav) OH O + H 20 fenol H30 + fenolát anionok O O O válasz: A keletkező fenolát anion konjugáció révén stabilizálódik, az egyensúly ezért ennek javára eltolódik kérdés: hogyan befolyásolják a szubsztituensek a fenol kémhatását? memo: a p-krezolban a konjugáció kb. annyira kiterjedt mint a fenolban, de a p-nitrofenolban viszont kiterjedtebb, ami tovább növeli a savas karaktert. memo: az eltérő savasság eltérő vízoldhatóságot eredményez: pKa = 9.9 (fenol), 16 (víz), 18 (ciklohexanol) OH O +
NaOH erõsebb sav gyengén vízoldható H 20 a fenolok disszociációja vízben 10000-szerese a + HOH ciklohexanolénak töltött részecskék megjelenése megnövekedett oldhatóság gyeng bázis Na vízoldható OH O Na + NaOH gyengébb sav alig vízoldható H20 + H2O erõsebb bázis vízoldható OH OH OH kétértékű fenolok: három különböző izomer OH OH rezorcin Benzene-1,3-diol pirokatechin Benzene-1,2-diol háromértékű fenolok: három különböző izomer OH OH OH OH OH HO OH pirogallol Benzene-1,2,3-triol benzol-1,2,3-triol naftolok: OH oxihidrokinon Benzene-1,2,4-triol benzol-1,2,4-triol OH •redukáló-szer: AgNO3 – fotó előhívás •„depigmentáció” OH f loroglucin Benzene-1,3,5-triol benzol-1,3,5-triol OH OH 1-naftol (a-naf tol) 1-Naphthol antrolok: OH hidrokinon Benzene-1,4-diol 2-naf tol (-naftol) 2-Naphthol OH 1-antrol (a-antrol) 9-antrol (antranol) 1-Anthrol 9-Anthrol memo: rendhagyó nevezéktan
1-naftol és nem naft-1-ol 1-antrol és nem antr-1-ol fenantrolok: 2-fenantrol 2-Phenanthrol HO OH OH Nev. gyak OH OH Br CH3 CH3 OH Br H2C NO2 2,4-dibrómfenol 2,4-Dibromophenol 4-nitrofenol (p-nitrofenol) 2-Methylbenzene-1,3-diol 2-metilbenzol-1,3-diol CH3 4-etil-2-metilfenol 4-Ethyl-2-methylphenol 4-Nitrophenol Példa: OH 4-(2-Amino-1-hydroxyethyl)benzene-1,2-diol 4-(2-amino-1-hidroxietil)benzol-1,2-diol noradrenalin OH OH OH CH2 CH NH2 COOH OH OH 2-Amino-3-(3,4-dihydroxyphenyl)propionic acid 2-amino-3-(3,4-dihidroxifenil)propionsav CH 4-(2-Amino-1-hydroxyethyl)benzene-1,2-diol 4-(2-amino-1-hidroxietil)benzol-1,2-diol noradrenalin stressz hormon, OH CH2 NH2 neurotranszmitter, gyógyszerként: vérnyomás emelő OH OH DOPA 3,4-dihidroxyphenylalanine neurotranszmitter prekurzor: dopamin, + Parkinson-kór kezelése CH2 CHnoradrenalin NH2 2. Aromás alkoholok: CH2OH CH2OH OH CH2OH CH C fenilmetanol Phenylmethanol OH (2-Hydroxymethyl)phenol
trif enilmetanol (2-hidroxibenzil)-alkohol Triphenylmethanol szalicilalkohol, szaligenin benzil-alkohol benzylalcohol 3. Fenoléterek: OCH3 HC H 2C CH3 CH2OH 3-Phenyl-prop-2-en-1-ol 3-fenil-prop-2-én-1-ol fahéjalkohol 2-Phenylethan-1-ol 2-feniletan-1-ol fenetil-alkohol OCH3 CH H2C H2C O O H2C anizol metoxibenzol fenil-metil-éter Methoxybenzene CH2 etoxibenzol etil-fenil-éter Ethoxybenzene (alliloxi)benzol allil-fenil-éter (Allyloxy)benzene Fenoléterek előállítása: Savas jellegük miatt már NaOH-dal is fenolátot képeznek (Williamson szint.), míg az alkoholok csak fém Na-mal adnak alkoholátot! CH CH2 esztragol 1-allil-4-metoxibenzol 1-Allyl-4-methoxybenzene OH CH3 O Na OC2H5 NaOH C2H5-I -H2O -NaI H3C CH3 4. Kinonok: már nem aromás vegyületek +1 +2 +1 +2 memo: könnyen oxidálhatók a fenolok és redukálhatók a kinonok hidrokinon memo: A fekete-fehér fényképezés során a lemezre rétegelt AgBr szemcséket fénnyel
aktiváljuk. Előhíváskor a hidrokinon redukálja az Ag + fém Ag-é, ami fekete szemcseként rögzül a negatívon és ami a „negatív kép” sötét része. hidrokinon HO 1,4-benzokinon OH + AgBr* O O + 2Ag + 2HBr memo: neve kinon de nem kinoidális szerkezetű a molekula OH Példák: CH3 HO O O H C H kámforkinon flavanon [NÉT1 198] OH O O 1,7,7-Trimethylbicyclo[2.21]heptane-2,3-dione 1-Methylbicyclo[2.21]heptane-2,3-dione 5,7-Dihydroxy-2-(4-hydroxyphenyl)chroman-4-one kámforkinon - fogtömések egyik komponense O CH3 K2 vitamin CH3 CH2 CH O 2-Methyl-1,4-naphthoquinone C [Stryer 255] CH2 H 6 szükséges a protrombin és más kalciumkötő fehérjék szintézisénél (vérkoagulációs hatás), gyermekkorban: egészséges csontfejlődés O H3C plasztokinon A oxidált forma ( a redukáltf orma a hidrokinon) [NÉT1 57], Stryer 659 H3C O 2,3-Dimethyl-1,4-benzoquinone 9 fotoszintézis: fény hatására vízből O2-t fejlesztve redukálódik a
plasztokinon A A mitokondrium oxidáló szere: Koenzim Q és NADH az oxidációs rendszer nélkülözhetetlen részei O CH3O -2 CH3 +2 CH3O CONH2 N cukor R O + H+ NADH redukált Koenzim Q oxidált H H H CH3O OH -1 CH3 +1 CH3O R Koenzim Q redukált XI. Aromás kénvegyületek SH HS SH CH2 SH CH3 Benzenethiol benzoltiol tiofenol cukor OH R:= 10 izoprén egység (membránba horgonyzás) 1. Tiolok N Br 3-Methylbenzene-1-thiol Phenylmethanethiol 4-Bromobenzene-1-thiol fenilmetántiol 3-metilbenzol-1-tiol 4-bróm-benzol-1-tiol m-tiokrezol p-brómbenzol-1-tiol NAD+ oxidált CONH2 S S 2. Szulfidok CH3 difenil-szulfid diphenyl sulfide Methylsulfanylbenzene metil-fenil-szulfid methyl phenyl sulfide 3. Szulfoxidok 4. Szulfonok O O S S C3H7 O fenil-propil-szulfon phenyl propyl sulfone difenil-szulfoxid diphenyl sulfoxide 5. Szulfonsavak SO3H SO3H CH3 benzolszulfonsav Benzenesulfonic acid p-toluolszulfonsav Toluene-4-sulfonic acid 6.
Szulfonsav-észterek SO3H SO3CH3 4-aminobenzolszulfonsav 4-Aminobenzenesulfonic acid SO3H COOH Methyl benzenesulfonate metil-benzolszulfonát Benzenesulfonic acid methyl ester benzolszulfonsav-metil-észter 7. Szulfonsav-kloridok, szulfonsav-amidok 4-Sulfobenzoic acid 4-szulfobenzoesav p-szulfobenzoesav NH2 tozil-klorid p-toluolszulfonil-klorid 4-Methylbenzenesulfonyl chloride 4-metilbenzolszulfonil-klorid SO2Cl SO2NH2 SO2Cl CH3 benzolszulfonil-klorid Benzenesulfonyl chloride CH3 p-toluolszulfonamid Toluene-4-sulfonamide XII. Aromás nitrogéntartalmú vegyületek Előtag: nitro-, nitrozo- 1. Aromás niro- és nitrozovegyületek típusnév: nitro-arén, nitrozo-arén NO2 NO2 O2N nitrobenzol Nitrobenzene O2N 1,3-dinitrobenzol m-dinitrobenzol 1,3-Dinitrobenzene NO2 NO2 NO2 O2N 1,3,5-trinitrobenzol CH3 1,3,5-Trinitrobenzene 2,4,6-trinitrotoluol (TNT, trotil) 2,4,6-trinitrotoluene O2N NO NO2 NO2 CH2 1-nitronaftalin (a-nitronaftalin) 1-Nitronaphthalene
nitrozobenzol Nitrosobenzene fenilnitrometán Phenylnitromethane Néhány „robbanékony” nitrobenzol származék: OH O 2N NO2 ammónium-pikrát NO2 Trinitrotoluol (TNT) Pikrinsav (sói a pikrátok) kémcső kísérlet (max. 1g anyaggal) memo: fokozottan explozívak a TNT szubsztituált származékai pl.: trinitro metakrezol (ekrazit) pl. memo: tárolási, stabilitási okok miatt NH3 sói formában használjuk trinitrofluroglucin (TNFG) memo: hevesebb mint a TNT tetranitro-N-metilanilin (tetril) memo: még hevesebb gyutacsnak használták vas-pikrát (igen explozív) kémcsöves kísérlet TILOS! max. 1g anyag 2. kísérlet: süvítve kilő 1. kísérlet: gyűrtpapír! alufólia gyújtópálcával vagy gyufával a papírt meggyújtjuk Bunsen-égő 1. 2. TNT pikrinsav kormozó láng kilő TNFG heves, sistereg TILOS „tetril” még fényesebb TILOS fekete lőpor (Kina XI. század tűzijáték): helyes aránya a szénpor (tüzelőanyag) + kén
(tüzelőanyag) + salétrom (KNO3 oxidálószer) keverékének. Robbanásszerű térfogatnövekedés (pl. CO2) bizt a tolóerőt memo: Stroncium-nitrát segítségével vörösre, bárium-nitrát révén zöldre, réz-karbonáttal pedig kékre lehet változtatni a robbanás színét. füst nélküli lőpor: cellulóz nitrát szilárd hajtóanyag: Al és NH4ClO4 (ammónium-perklorát) (űrtechnika) gyufafej: KClO3 (kálium-klorát oxidálószer) + szénpor, kén és antimonszulfidok (Sb2S3 és Sb2S5 narancssárga) (tüzelőanyagok) keveréke. Égés során keletkező gázok: pl. CO2, SbO, SO2 memo: a gyufásdoboz dörzsfelületén vörös foszfort (P4) van, ami a súrlódás hatására könnyen meggyullad, azaz iniciátor. Robbanószerek jellemzése, az oxigénmérleg: kérdés: hány O2 molekula kell a szerves anyag elégetéséhez, ha azt feltételezzük, hogy CO2, N2, H2O keletkezik? 2 C3H5N3O9 – ½ O2 = 6 CO2↑ + 5 H2O↑ + 3 N2↑ CH2 O NO2 CH O NO2 CH2 O Alfred
Nobel egy mol. belül van mind a NO2 csop (oxidálószer) 1833-1896 mind a CH2 és CH (tüzelőanyag). Ezért igen hatékony! Összesen 14 mol gáz és gőz keletkezik: kvázi nullszaldós oxigénmérleg NO2 nitroglicerin (színtelen foly.) dinamit: diatomaföldbe (kovaföld, üledékes kőzet) felitatott nitroglicerin 2 C7H5N3O6 + 10,5 O2 = 14 CO2↑ + 5 H2O↑ + 3 N2↑ „TNT” 22 mol gáz és gőz keletkezik 2 C6H3N3O9 + 4,5 O2 = 12 CO2↑ + 3 H2O↑ + 3 N2↑ 18 mol gáz és gőz keletkezik „TNFG” 2. Aromás aminok és iminek típusnév: arilamin , arilimin H Ar Ar Ar N Ar H primer aromás amin (aril-amin) Ar N N H Ar szekunder aromás amin (diaril-amin) tercier aromás amin (triaril-amin) A. Egyértékű primer aminok NH2 NH2 NH2 NH2 H 3C CH3 anilin NH2 o-toluidin m-toluidin CH3 NH2 NH2 OH 2-aminof enol o-aminof enol 2-Aminophenol 1-naftil-amin (a-naftil-amin) 2-naftil-amin (-naftil-amin) p -toluidin B. Egyértékű szekunder
aminok H N H N bisz(2-naftil)-amin Bis(2-naphthyl)amine difenil-amin Diphenylamine H3C C. Egyértékű tercier aminok C6H5 C6H5 CH3 N N C6H5 trifenil-amin N ,N-dimetilanilin N ,N-Dimethylaniline Triphenylamine D. Kvaterner ammóniumvegyületek CH3 H3C OH N H3C CH2 Cl H3N benzil-trimetil-ammónium-hidroxid Benzyltrimethylammonium hydroxide anilinium-klorid anilinium chloride E. Többértékű aminok naf talin-1,4-diamin Naphthalene-1,4-diamine NH2 NH2 NH2 NH2 p -fenilén-diamin p -Phenylenediamine Benzene-1,4-diamine NH2 NH2 bifenil-4,4'-diamin Biphenyl-4,4'-diamine F. Aromás iminek CH3 HC HN CH N benzilidénimin Benzylideneimine N-etilidénanilin N-Ethylideneaniline 3. Aromás hidroxilamin és hidrazinszármazékok típusnév: aril-hidroxilamin Utótag: hidroxilamin Előtag: hidroxilamino HO NH HO C2H5O NH NH OH N -fenilhidroxilamin 4-(hidroxiamino)fenol N-Phenylhydroxylamine 4-(Hydroxyamino)phenol O-Ethyl-N-phenylhydroxylamine
O-etil-N-f enilhidroxilamin Utótag: hidrazin Előtag: hidrazino típusnév: aril-hidrazin CH3 HN NH2 fenilhidrazin Phenylhydrazine NH2 HN NH HN N-metil-N ,-fenilhidrazin OH 4-hidrazinofenol N-Methyl-N'-phenylhydrazine 4-Hydrazinophenol 4. Aromás azo- és azoxivegyületek típusnév: azoarén Előtag: azo Utótag: diazén N Szimmetrikus aromás azovegyület N difenildiazén Diphenyldiazene azobenzol azobenzene Aszimmetrikus aromás azovegyület N 4 1 H2N CH3 N C6H5 N 4-(fenilazo)toluol 4-(phenylazo)toluene Phenyl-p-tolyldiazene fenil-p-tolildiazén N 1 C6H5 N N 4 1 N C6H5 N 4-(fenilazo)benzol-1,3-diamin 4-(Phenylazo)benzene-1,3-diamine N (krizoidin)N NH2 NH2 NH2 1-(fenilazo)naftalin-2-amin 1-(Phenylazo)naphthyl-2-amine NH2 4-(fenilazo)naftalin-1-amin 1-(fenilazo)naftalin-2-amin 4-(Phenylazo)naphthyl-1-amine 1-(Phenylazo)naphthyl-2-amine C6H5 N N 4 1 NH2 4-(fenilazo)naftalin-1-amin 4-(Phenylazo)naphthyl-1-amine kérdés: mi lehet a szín
molekuláris oka? válasz: a megfelelő kromofor csoport nyeli el a fényt - a finomhangolást a konjugáció kiterjedésének mértéke biztosítja memo: chroma = szín, phoros = hordozó (görög) itt: konjugált kettős-kötés rendszer sárga 4-nitroazobenzol N elnyelés: 420-430nm O N N kérdés: miért lehet színes egy azovegyület? memo: a fehér fény (400-800 nm) 2 1. – teljes spektrumból szelektíven nyel el egy tartományt 2. – a megmaradó komponensek O2N keverék színét érzékeljük sárgásvörös 4-nitro-4’-aminoazobenzol NH2 N N CH3 N N O2 N N CH3 sötétvörös 4-nitro-4’-(N,N-dimetilamino)azobenzol elnyelés: 500-520nm memo: más kromofórok is finomhangolhatók pl. konjugált ketonok Otto Nikolaus Witt 1853-1915 H3C aceton színtelen C O O H 3C CH3 C H 3C O C O biacetil H3C sárga C CH3 C C O O 2,3,4-triketopentán narancssárga Példa: HO H2N NH2 4 H2N NH2 2 N N N N N N HO HO3S 1,3- bisz[ (2,4-d iaminof enil)
azo ]-be nzol (Bismarc k-b arn a) SO3H N N HO3S 4-(2-hidro benzolszul 4-(2-Hydro ben (-naftolo 4-(2-hidroxinaftalin-1-ilazo)benzolszulfonsav 4-(2-Hydroxynaphthalen-1-ylazo)benzenesulfonic acid (-naftoloranzs 450-510nm) N N NH2 NH2 N N 4,4,-bisz(1-amino-4-szulfonaftalin-2-ilazo)bifenil (kongóvörös: legerõsebb sáv 400-560nm között) SO3H Congo Red: a strong absorption band at 340nm (near-UV) and another at 500nm (at blue-green transition region). This dye transmits red wavelengths above 560 nm and thus, appears red to the eye. azoxivegyületek COOH O N N N N O N,N '-Diphenyldiazene N -oxide N,N'-difenildiazin-N -oxid azoxibenzol 2-(Phenyl-O,N,N-azoxy)naphthalene-1-carboxylic acid 2-(fenil-O,N,N -azoxi)-1-naftalin-1-karbonsav 5. Aromás diazónium vegyületek típusnév: aréndiazonium N2 N2 Cl Előtag: diazónio Utótag: diazónium OH N2 8 1 BF4 SO3 benzoldiazonium-klorid Benzenediazonium chloride 8-hidroxinaftalin-1-diazonium
tetrafluoroborát 4-diazoniobenzol-1-szulfonát 4-Diazoniobenzene-1-sulfonate 8-Hydroxynaphthalene-1-diazonium tetraf luoroborate A diazónium kation fontos poláris határszerkezetei: N N N N N N N N N N Bruckner II/1 565 A benzoldiazónium-klorid előállításának részletei: Itt nincs meg az elektron-oktett!: potens elektrofil a bruttó reakció: néhány részlet: N-nitrozo-ammónium kation arilamin H N H H N O -H+ N N O H N N OH -H2O +H Bruckner II/1 569 N N Diazónium kation Diazohidroxid H N N O N-nitrozoamin Aromás diazónium vegyületek tipikus reakciói: gyökös Sandmeyerszerű reakciók: „azokapcsolás” : Cl OH N N H Cu2O, Cu2+, H2O Ar Cl OH SE OH CuX X=Cl, Br, CN N2 Ar Cl X N N KI Ar N3 I H N3 -HX HBF4 + hõ Ar OH F N H3PO2 + H2O N Ar H 6. Aromás azidovegyületek típusnév: azidoarén és aril-azid Szn Csn N3 Előtag: azido Utótag: nincs Az azidobenzol két poláris
határszerkezete: N3 SO3H instabil robbanékony f enil-azid Azidobenzene azidobenzol 1-azidonaftalin-2-szu f enil-azid azobenzol származékok (szinezékek) 1-Azidonaphthalene-2 Azidobenzene azidobenzol elektrofil szubsztitúció 1-azidonaftalin-2-szulfonsav 1-Azidonaphthalene-2-sulfonic acid N N N N N N XIII. Aromás oxovegyületek 1. Aromás aldehidek - típusnév: arilaldehid Képzés: az arilkarbonsav nevének megfelelő csonkított acilnévből az pl.: ftáloil ftálaldehid, naftoil naftaldehid Triviális savnév esetén csonkított acilnév + aldehid pl.: benzoil +aldehid benzaldehid A gyűrűhöz közvetlenül csatlakozó aldehideket karbaldehideknek hívjuk pl.: naftalinkarbaldehid aldehid utótaggal képezzük A) Karbaldehidek CHO CHO CHO OH OH 2-hidroxibenzaldehid 2-Hydroxybenzaldehyde 3-hidroxibenzaldehid 3-Hydroxybenzaldehyde CH3 4-metilbenzaldehid 4-Methylbenzaldehyde Előtag: formil Utótag :karbaldehid Példa: CHO CHO 2 CHO HC
CH 3 OCH3 OH 4-hidroxi-3-metoxibenzaldehid vanillin OCH3 3-fenilakrilaldehid fahéjaldehid 4-Hydroxy-3-methoxybenzaldehyde 3-Phenylprop-2-enal B) Alifás oldalláncú aromásaldehidek CHO CHO CH H2C CHO [(1-naftil)metil]-malonaldehid H2C (1-naftil)acetaldehid 4-metoxibenzaldehid ánizsaldehid 4-Methoxybenzaldehyde 2. Aromás ketonok Szn.: előtag: oxo típusnév: alkanon utótag: on Csn.: keton C O A) az alifás oldallánc része az O karbonilcsoport oxocsoport H3C H3C C O O O CH2 CH3 CH O2 CH2 CH2 CH3 O C CH3 CH O2 CH2 C CH3 O 1-Phenylbutan-2-one O 1-Phenylpropan-2-one 1-Phenylethan-1-one 1-fenilpropán-2-on 1-fenilbután-2-on 1-feniletan-1-on 1-f enilbutan-2-on f enilaceton acetof enon 1-Phenylbutan-2-one 1-Phenylpropan-2-one 1-Phenylethan-1-one fenil-metil-keton benzil-etil-keton benzil-metil-keton 1-fenilpropán-2-on 1-fenilbután-2-on 1-feniletan-1-on methyl-phenyl keton 1-f enilbutan-2-on f enilaceton acetof enon B) Az karbonilcsoport két
aromás gyűrűhöz benzil-etil-keton kapcsolódik fenil-metil-keton benzil-metil-keton O methyl-phenyl keton O Szn. Csn. C Csn. fenil-(2-naftil)-keton Szn. Naphthalen-2-yl-phenyl-methanone C benzofenon difenil-keton difenilmetanon Diphenylmethanone C) Aromás di-, tri- és poliketonok O C D) Aromás rendszerekhez integrálódott ketonok O O C C O C inden-1-on C C Inden-1-one O O dif enil-diketon 1,2-Diphenylethane-1,2-dione 1,2-difeniletán-1,2-dion f luorén-9-on bisz(2-naf til)-diketon O Di(2-naphthyl)ethane-1,2-dione C di(2-naftil)etán-1,2-dion CH2 Fluoren-9-one O O C C 1,2-dihidronaftalin-1-on 9 10 1,2,-Dihydronaphthalen-1-one CH2 C O Csn. bisz(2-naf til)-diketon Di(2-naphthyl)ethane-1,2-dione Szn. di(2-naftil)etán-1,2-dion memo: H2 C 1 2 CH2 1,2-Dihydronaphthalene 1,2-dihidronaftalin antron 9,10-dihydroanthracen-9-one 9,10-dihidroantracén-9-on XIV. Aromás karbonsavak: Az aszpirin rövid története - A fűzfakérget az ókori
Ázsiában is használják (2400 éve) láz és fájdalomcsillapításra, - 1830-tól a fűzfakéreg extraktumát használják hasonló célból, - 1840 körül azonosítják a kivonat aktív komponensét a szalicint (salix [latin] fűzfa) - 1870 Nencki (Bázel) kimutatja hogy a szervezetben szalicilsavvá alakul át a szalicin (a szalicilsav is fájdalom és lázcsillapító, de égeti a nyelőcsövet, gyomrot) - 1875 Patikusok elkészítik a Na+ sóját, „működik”, de borzasztó az íze, hánytat - 1890 Félix Hofmann/Arthur Eichengrün(??) (Bayer) elkészíti az aszpirint, ami jól hat és elfogadható ízű: „a” acetilt, „spir” spirea-t (gyöngyvessző melyből szalicilsav-metilészter izolálható) - 1898 Az aszpirin klinikai kipróbálása és üzemi gyártása (Bayer) - 1990 Csak az USA-ban > 10 millió kg-t gyártanak évente Hatásmechanizmus: az aspirin, mint acetilezőszer a ciklooxigenáz (COX) inhibitora, gátolja a szintézist) prosztaglandin -
gyulladáscsökkentő, - a köszvény és reuma hatásos gyógyszere Ciklooxigenáz-arahidonsav komplex Loll, P.J, Picot, D, Garavito, RM (1995) NatStructBiol 2: 637-643 Harman, C.A, Rieke, CJ, Garavito, RM, Smith, WL (2004) JBiolChem 279: 42929-42935 H2N Ser H2N O Ser-Ac O O CH2 OH CH3 CH2 Szerin TreoninC OH H2N O CH C OH SH O C O O O C 2N CCH OH OH H2N HCH C HCH CH C OH H2N CH 2N OH CH2 CH2 CH C OH H2N C OH C CH OH2 C O CiszteinSzerin NH CH2 3 C N O H2N T Szintézis tervezet: a fenolból aszpirin Bruckner: II/703 II/726 II/860 kőszén, petróleum memo: gyomorban nem, bélben hidrolizál (ecetsav + szalicilsav) Kolbe-szintézis: / 100 atm memo: az aszpirin gátolja a ciklooxigenázt, amely prosztaglandin szint. része, így ennek csökkenése a fájdalomküszöböt növeli és a gyulladást csökkenti. XIV. Aromás karbonsavak Az aromás gyűrűhöz kapcsolódó vagy annak oldalláncában a láncvégi metilcsoport hidrogénjeit
cseréljük: 2 db H-t O-ra; 1 db H-t OH-ra karboxilcsoport kapcsolódása szerint: arénkarbonsav arilezett alifás karbonsav karboxilcsoportok száma szerint: egy-, két-, három- és több-bázisú sav szénhidrogén oldallánc: telített telítetlen Előtag: karboxi Utótag :karbonsav Nostradamus (1556) 1. Arénkarbonsavak típusnév: arénkarbonsav COOH A. Egyértékű savak: tartósítószer (gombák, baktériumok benzolkarbonsav szaporodását gátolja): benzoesav E210, E211, E212, E213 Benzoic acid COOH 1 2-naf toesav 2-naphtoic acid COOH COOH COOH COOH CH3 2 3 H3C 2-metilbenzoesav o-toluilsav 3-metilbenzoesav m-toluilsav 2-Methylbenzoic acid 3-Methylbenzoic acid 1 4 COOH 2-naf toesav CH3 2-naphtoic acid 4-metilbenzesav p-toluilsav 4-Methylbenzoic acid 1 1-naf toesav 1-naphtoic acid B. Kétértékű savak: COOH COOH COOH HOOC 1 4 1 2 3 COOH COOH COOH COOH COOH 1,4-benzoldikarbonsav benzene-1,4-dicarboxylic acid o tereftálsav
COOH HOOC op=425 COOH Terephthalic acid grafit szerkezetigazoló benzol-1,2.3-trikar benzol-1,3,5-trikarbonsav oxidációja (hemimellitsav) kérdés: miért ennyire eltérő a három szerkezeti izomer(trimezinsav) olvadáspontja? Benzene-1,3,5-tricarboxylic acid Benzene-1,2,3-tric benzol-1,2-dikarbonsav benzene-1,2-dicarboxylic acid op=231o ftálsav Phthalic acid benzol-1,3-dikarbonsav benzene-1,3-dicarboxylic acid op=348o izof tálsav Isophthalic acid memo: intermolekuláris H-hidak Bruckner II/1 799 COOH C. Többértékű savak: COOH COOH HOOC COOH HOOC COOH COOH HOOC COOH COOH benzol-1,2.3-trikarbonsav benzol-1,3,5-trikarbonsav (hemimellitsav) (trimezinsav) Benzene-1,3,5-tricarboxylic acid Benzene-1,2,3-tricarboxylic acid COOH benzol-1,2,3,4,5,6-hexakarbonsav (mellitsav) Benzene-1,2,3,4,5,6-hexacarboxylic acid O D. peroxisavak: O O C H C O perbenzoesav peroxibenzoesav perbenzoic acid O O H O H C diperoxi-ftálsav O O rossz a benzolperoxikarbonsav
mert rossz a benzol-1,2-diperoxikarbonsav a benzolkarbonsav név sem használható a benzoesav helyett mert af tálsav helyett nem mondhstjuk hogy benzol-1,2-karbonsav 2. Arilezett alifás karbonsavak Előtag: karboxi típusnév: arilalkánsav A. Telített oldalláncú: Utótag :sav H3C 2 COOH CH 3 CH2 COOH CH2 CH2 COOH f enilecetsav Phenylacetic acid 3-fenilpropánsav hidrof ahéjsav 2-fenilpropánsav hidratropasav 3-Phenyl-propanoic acid 2-Phenyl-propanoic acid konstitúciós izomerek B. Telítetlen oldalláncú: H2C COOH C 2-fenilakrilsav (atropasav) H H C C 2-Phenylacrylic acid C C H nev. gyak H2 H2 H3C 5 C 3 C CH CH COOH 1 H COOH cisz-3-fenilpropénsav (allofahéjsav) transz-3-fenil-propénsav (f ahéjsav) 3-Phenylacrylic acid 3-Phenylacrylic acid CH3 sztereo izomerek HOOC CH2 3-metil-5-(1-naftil)hexánsav 3-Methyl-5-(1-naphthyl)hexanoic acid 5 1 HOOC COOH H2 C 3 C H2 COOH 3-(2-karboxietil)-5-(karboximetil)benzoesav
3-(2-Carboxyethyl)-5-(carboxymethyl)benzoic acid 3. Magban szubsztituált arénkarbonsavak Előtag: karboxi COOH Utótag :karbonsav típusnév: arilkarbonsav COOH COOH COOH COOH Cl 1 O2N Cl H 2N NO2 1 COOH 1 1 NH2 2-klórbenzoesav o-klórbenzoesav 2-Chlorobenzoic acid 2-aminobenzoesav 4-aminobenzoesav p-aminobenzoesav o-aminobenzoesav 2-nitrobenzoesav 1-klórnaftalin-2-karbonsav (antranilsav) o-nitrobenzoesav 1-Chloronaphthalene2-Aminobenzoic acid 4-Aminobenzoic acid 2-Nitrobenzoic acid 2-carboxylic acid H 2N COO NO2 2,4,6-trinitrobenzoesav 2,4,6-Trinitrobenzoic acid COOH IkerionosCOOH szerkezet: COOH NO2 protonCOOH O2N H 2N COOH NO2 H 3N 4 2 NH2 NH2 2-aminobenzoesav o-aminobenzoesav (antranilsav) 2-Aminobenzoic acid 4-aminobenzoesav p-aminobenzoesav 4-Aminobenzoic acid NO2 2-aminobenzoesav o-aminobenzoesav 2,4,6-trinitrobenzoesav (antranilsav) 2,4,6-Trinitrobenzoic acid acid 2-Aminobenzoic =7.58 Debye 4-aminobenzoesav p-aminobenzoesav
4-Aminobenzoic acid COOH COOH COOH COOH OH HO OCH3 OH 2-hidroxibenzoesav o-hidroxibenzoesav (szalicilsav) OH 3,4,5-trihidroxibenzoesav (galluszsav) 2-Hydroxybenzoic acid 3,4,5-Trihydroxybenzoic acid OH 4-hidroxi-3-metoxibenzoesav (vanillinsav) 4-Hydroxy-3-methoxybenzoic acid OCH3 4-metoxibenzoesav p-metoxibenzoesav (ánizssav) 4-Methoxybenzoic acid 4. Arilezett alifás karbonsavak szubsztituált származékai COOH típusnév: aralkilsav (pl. akrilsav szárm : CH2=CHCOOH) Előtag: karboxi COOH COOH Utótag :karbonsav C H H H C C H H OCH3 C C HOOC OH H OCH3 C OH OH 3,4-dimetoxibenzoesav (verátrumsav) 3,4-Dimethoxybenzoic acid OH 3-(2,4-dihidroxifenil)akrilsav 3-(2-hidroxifenil)akrilsav (kávésav) transz (o-kumársav) transz 3-(2-hidroxifenil)akrilsav (o-kumarinsav) cisz 3-(2,4-Dihydroxyphenyl)acrylic acid 3-(2-Hydroxyphenyl)acrylic acid 3-(2-Hydroxyphenyl)acrylic acid nev. gyak O C 3 CH2 3 COOH 2-amino-3-(4-hidroxif enil)propánsav
(4-hidroxif enil)-alanin vagy tirozin C H NH2 2-Amino-3-(4-hydroxyphenyl)propanoic acid CH2 COOH 4-oxo-4-fenilbutánsav CH2 4-Oxo-4-phenylbutanoic acid OH 3-benzoil-propionsav O C O H2C C 5 3 H C COOH 3,5-dioxo-2-fenilvaleriánsav H 3,5-dioxo-2-f enilpentánsav 3,5-Dioxo-2-phenylpentanoic acid O O 5. Aromáskarbonsavak funkcionális származékai O C O O O O CH3 benzoesav-anhidrid O C O H2 O O O O A. Karbonsavanhidridek: O O benzoesav-anhidrid C benzoe CH C ftálsav-anhid H2 1,3-dihidrobe (ftálsavból hevítésre k Cbenzoesav-propionsav-an O ftálsav-anhidrid 1,3-dihidrobenzof urán-1,3-dion benzoesav-propionsav-anhidridO C (ftálsavból hevítésre könnyen képzõdik) B. Karbonsavészterek:O (o-dikarbonsav) O ftálsav-anhidrid O O CH3 C O C CH2 1,3-dihidrobenzof urán-1,3-dion dimetil-ftalát C CH3 O dimethyl phtalate O képzõdik) Bruckner II/ 1 825 C (ftálsavból hevítésre könnyen Ethyl benzoate Phthalic acid dimethyl ester etil-benzoát
O O C CH3 Benzoic acid ethyl ester benzoesav-etil-észter O benzoesav-anhidrid Csn COOCH3 O C O CH2 antracén-9-karbonsav-metil-észter Anthracene-9-carboxylic acid methyl ester ftalid 3H-Isobenzofuran-1-one COCl C. Karbonsavhalogenidek: COCl COCl OH szalicilsav-klorid COCl COCl (2-Hydroxybenzoyl) chloride (2-hidroxibenzoil)-klorid OCH3 benzoil-klorid Benzoyl chloride ftaloil-diklorid (4-Methoxy)benzoyl chloride (4-metoxi)benzoil-klorid Phthaloyl dichloride ánizssav-klorid CH3 D. Karbonsavamidok: CONH2 C NH O Phtalamic acid CONH2 CONH2 acetanilid COOH N-Phenylacetamide CONH2 benzoesav-amid benzamid tereftálsav-amid tereftálamid ftálamidsav Benzamide Terephthalamide Phthalamic acid O C O NH C ftálimid CH3 O Isoindole-1,3-dione NH C N-metilbenzamid N -Methylbenzamide E. Karbonsavnitrilek: CN CN CN benzonitril Benzonitrile benzoesavnitril ftalonitril Phthalonitrile ftálsav-dinitril NC fenil-izocianid Isocyanobenzene memo: ez nem nitril
hanem izocianid




 When reading, most of us just let a story wash over us, getting lost in the world of the book rather than paying attention to the individual elements of the plot or writing. However, in English class, our teachers ask us to look at the mechanics of the writing.
When reading, most of us just let a story wash over us, getting lost in the world of the book rather than paying attention to the individual elements of the plot or writing. However, in English class, our teachers ask us to look at the mechanics of the writing.